Bienvenido a nuestra Biblioteca Clínica
Clinical Library
26
Daño celular intestinal y respuesta inmune sistémica en individuos con sensibilidad al gluten no celíaca
A pesar del aumento del interés de la comunidad médica en esta entidad, la etiología y el mecanismo de la sintomatología es desconocido, y los biomarcadores todavía no han sido identificados. No se dispone de cifras de prevalencia, aunque sí se estima que es similar o superior a la de la enfermedad celíaca (EC).
En el presente estudio se investiga:
- Si la respuesta inmune sistémica en respuesta a los productos generados en la translocación bacteriana puede ser una característica de la SGNC.
- Si esta respuesta inmune sistémica está relacionada con un compromiso del epitelio intestinal.
- Si la respuesta inmune sistémica y la lesión del epitelio intestinal responden positivamente ante la eliminación del trigo y cereales similares de la dieta.
>>>Leer artículo original<<<

Anemia en la enfermedad celíaca en edad pediátrica: asociación de características clínicas e histológicas y respuesta a una dieta libre de gluten
Journal of Paediatric Gastroenterology and Nutrition, e-pub ahead of print, Marzo2016
La enfermedad celíaca (EC) es uno de los trastornos gastrointestinales más comunes en los niños. Una de las manifestaciones más habitual de la EC en pediatría es la anemia por déficit de hierro. Incluso una anemia leve o subclínica puede ser perjudicial para la salud, ya que predispone a un pobre desarrollo cognitivo y psicomotor y al deterioro de la defensa inmune. Este estudio retrospectivo comparó una variedad de características clínicas, histológicas, serológicas, hallazgos de laboratorio y la respuesta a la dieta entre los niños que presentaban anemia y los que no en el momento del diagnóstico de EC.
>>Leer artículo original<<

Eficacia de una dieta sin gluten en sujetos con síndrome del intestino irritable (SII) / diarrea predominante y que desconozcan su genotipo HLA-DQ2/8.
Clinical Gastroenterolgy and Hepatology 2016, Artículo de prensa
El SII-D representa casi un tercio de los pacientes con SII y es el subtipo predominante del SII que más se encuentra en la práctica clínica. La investigación apunta a que un 84% de los pacientes con SII creen que la comida desencadena sus síntomas gastrointestinales y de estos, 1 de cada 4 citan la comida basada en el gluten como un desencadenante común. Estas observaciones han dado lugar a la entidad clínica conocida como sensibilidad al gluten no celíaca (SGNC). Sin embargo, la SGNC sigue siendo una condición controvertida debido a la existencia de componentes no-gluten co-existentes (incluyendo FODMAPs) que también han demostrado inducir síntomas en el SII.
El propósito de este estudio prospectivo fue evaluar la respuesta clínica de una cohorte de pacientes con SII-D ligado a su estatus desconocido de HLA-DQ y a una dieta sin gluten (DSG). El beneficio y la sostenibilidad a largo plazo de la dieta sin gluten también fueron evaluados.
El estudio se llevó acabo en el Royal Hallamshire Hospital, Sheffield, entre septiembre de 2012 y julio de 2015. Los pacientes que asistían a la consulta externa de gastroenterología y cumplían con los criterios Roma II para el SII-D fueron aptos para la inclusión en el estudio. La enfermedad celiaca fue excluida en base a una serología negativa y una biopsia duodenal normal. Los individuos con sensibilidad al gluten auto-diagnosticada, aquellos que ya llevaban una dieta sin gluten y aquellos con otros condicionantes médicos conocidos por “imitar” el SII-D también fueron excluidos. 68 pacientes fueron elegidos como aptos para el estudio, y de estos 48 accedieron a participar (24 HLA-DQ2/8+ y 24 HLA-DQ2/8-). Los sujetos fueron remitidos un dietista senior que les proporcionó información uniforme de cómo empezar una dieta sin gluten. A los sujetos se les entregaron cuestionarios validados para auto-cumplimentar el día antes de comenzar una dieta sin gluten y durante el periodo de dieta sin gluten, estos incluían el IBS Symptom Severity Score (IBS-SSS), Hospital Anxiety and Depression Scale (HADS), Fatigue Impact Score (FIS), y el Short-form 36 (SF-36) para la evaluación de la calidad de vida. Siete sujetos abandonaron el estudio (4 no asistieron a la consulta inicial con el dietista, 1 se quedó embarazada, 1 comenzó una dieta adicional, y a 1 la dieta sin gluten le parecía demasiado cara). A los sujetos restantes (21 HLA-DQ –; 20 HLA DQ +), se les mandó seguir una dieta sin gluten durante 6 semanas, después de la cual tuvieron una cita de seguimiento con el dietista y devolvieron sus cuestionarios. La fidelidad dietética fue evaluada usando una herramienta sencilla validada. A los pacientes también se les preguntó si tenían la intención de seguir con la dieta sin gluten en el futuro. Para aquellos que contestaron que sí, se les citó para realizarles un seguimiento de aproximadamente 18 meses después. Es importante advertir que ni los dietistas ni los pacientes sabían que el estatus HLA-DQ2/8 estaba siendo usado como comparativo dentro del estudio.
Tras seguir la dieta sin gluten durante 6 semanas, se vio una reducción en el cuestionario IBS-SSS de ≥50 puntos (indicando beneficios clínicos) en un 71% de los pacientes, sin haber diferencia entre grupos HLA-DQ. Se vio una reducción significativa de síntomas desde la semana 2 y continuaron cayendo en cada intervalo en la semana 4 y la semana 6. Las mayores mejorías se vieron en aquellos pacientes que tenían los marcadores de SII más graves en el punto de partida. Estudiando los submarcadores del SII, se observa una reducción media significativa en el dolor abdominal, la frecuencia de aparición de dolor, la insatisfacción a la hora de realizar deposiciones y las interferencias en la vida diaria en ambos subgrupos HLA-DQ, sin diferencias entre grupos. Sin embargo los sujetos HLA-DQDQ2/8- mostraron una mayor reducción en la distensión abdominal en comparación con los sujetos HLA-DQ2/8+ (p=0.04). También se observó una mejoría significativa tras una dieta sin gluten en ambos grupos, en HADS, FIS y el cuestionario SF-36 sobre la calidad de vida. Por otro lado, los pacientes HLA-DQ2/8+ experimentaron una mejoría significantemente mayor frente a la depresión (p=0.02) y una mayor vitalidad (p=0.03) comparado con el grupo HLA-DQ2/8-. Al final de la intervención de 6 semanas, el 72% de los pacientes que habían respondido positivamente al IBS-SSS tenían planeado seguir una dieta sin gluten en el futuro próximo (11 HLA-DQ2/8+ and 10 HLA-DQ2/8-). Cuando se contactó con estos pacientes tras una media de 18 meses después, todos seguían una dieta sin gluten con un buen nivel de fidelidad e informaron de una mejoría continuada de síntomas, sin alteraciones en el índice de masa corporal o estatus bioquímico (comparados con el punto de partido).
Los resultados de este estudio demuestran que una dieta sin gluten llevada por un dietista debería ser considerada como una opción terapéutica para el manejo de pacientes con SII-D, los cuales previamente desconozcan los efectos del gluten. Los puntos fuertes de este estudio son que su cohorte esta rigurosamente definida, que la enfermedad celiaca fue excluida y que los pacientes y dietistas desconocían el hecho de que el status HLA-DQ2/8 estaba siendo utilizado como un factor comparativo. Este estudio también se acopla una situación de vida real en la cual los pacientes recibieron una única consulta dietética y después se les dejó seguir la dieta sin gluten por si solos, en vez de darles todas las comidas en un ambiente de investigación fuertemente controlado. Las limitaciones del estudio incluyen el efecto placebo de comenzar un ensayo dietético, sin embargo es poco probable que esto explique la repuesta observada en el 71% de los casos, particularmente a la vista de que el bienestar se mantuvo a los 18 meses. Los autores de este estudio especulan con que los mecanismos fisiopatológicos que resultan en una reducción de síntomas para los pacientes con SII-D tratados con una dieta sin gluten pueden variar en función del estatus HLA-DQ, y que esto merece continuar siendo estudiado.
>>>Leer artículo original<<<

¿Es beneficiosa la dieta sin gluten en la esclerosis múltiple?
Hablar de EM significa hacerlo de un desorden inflamatorio crónico autoinmune que se caracteriza por la presencia de lesiones desmielinizantes diseminadas en el sistema nervioso central (SNC). Este trastorno afecta aproximadamente al 1% de la población, principalmente a mujeres jóvenes, y se encuentra asociado a otros trastornos autoinmunes como es la enfermedad celíaca (EC). Como se extrae del estudio de Rodrigo L et al., la EC aparece asociada a los pacientes que padecen EM en un 11% de los casos, lo que supone una frecuencia de entre 5 y 10 veces mayor que en la población general. También encontraron lesiones duodenales en el 29% de los pacientes de EM y una leve atrofia de las vellosidades en un 11.1%. Todo esto, junto con la alta prevalencia de EC en parientes de primer grado, hace pensar que la intolerancia al gluten esté implicada en la patogenia de la EM.
En las personas con EM se detectan cambios en anticuerpos frente a varios antígenos, presentando en ocasiones anticuerpos antigliadina y anti- tTG. La asociación entre estos anticuerpos y la EM fue ya indicada por Shor DB et al., quienes encontraron un aumento significativo de anticuerpos igG frente a la gliadina en pacientes con EM. Contrariamente a ésto, Borhani A et. al., no encontraron en ninguno de los 217 pacientes con EM estudiados presencia de igG ni igA anti- gliadina ni de anticuerpos anti-endomisio, lo que supuso que el aumento de la frecuencia de EC en pacientes con EM no quedase demostrada.
La relación del gluten con las manifestaciones neurológicas no está todavía clara, pero sí que se ha sugerido que la reacción autoinmune resultado del mimetismo entre la gliadina y las proteínas en el sistema nervioso tiene un papel importante.
Por todo ello, se decidió realizar la revisión de artículos científicos relativos a la EM y EC, para estudiar la posible relación entre ellas y sobre si debe o no considerarse la DSG en estos pacientes. Se debate si el consumo de gluten es un riesgo en la EM. Por un lado, no se encuentra suficiente armonía entre los resultados obtenidos en los distintos estudios realizados pero por otro, en el caso de pacientes con EM y EC, se detectó tras la revisión que los síntomas tanto físicos como neurológicos pueden mejorar a largo plazo con el seguimiento de DSG. Volta U et al., que estudiaron los síntomas en 160 pacientes, obtuvieron resultados que se traducían en la mejora o desaparición de los síntomas neurológicos en 7 pacientes que empezaron la DSG en los 6 primeros meses tras la aparición de los primeros síntomas. Estas conclusiones junto con otras obtenidas en otros estudios, sugieren que los trastornos neurológicos asociados a la EM podrían verse notablemente mejorados con el seguimiento de una DSG si ésta se comienza de forma temprana ante los primeros síntomas.
No obstante, se considera que es necesaria la continuación de ensayos de pacientes con trastornos múltiples autoinmunes para ayudar a identificar
Leer artículo completo

Diagnóstico de sensibilidad al gluten no celiaca en pacientes con síntomas gastrointestinales funcionales
Nutrients 2016; 8: 84; doi:10.3390/nu8020084
La sensibilidad al gluten no celíaca (sensibilidad al gluten o SGNC) es un trastorno caracterizado por síntomas intestinales y extraintestinales relacionados con la ingesta de alimentos que contienen gluten. Hoy en día, las analíticas sanguíneas y la histología disponible no ayudan a establecer un diagnóstico diferencial, por lo que, en ausencia de una enfermedad celiaca (EC) o de alergia al trigo (AT), la reacción a la dieta sin gluten es el principio fundamental para diagnosticar SGNC. Sin embargo, el efecto placebo sumado a la presencia de otros compuestos activos dentro del trigo, por ejemplo, los inhibidores de tripsina amilasa (ATI) y los FODMAP, pueden actuar como factores de confusión a la hora de analizar el impacto de la dieta sin gluten gluten entre aquellos que potencialmente padecen SGNC. Es crucial contar con un diagnóstico correcto, tanto para evitar restricciones dietéticas innecesarias, como para proporcionar un tratamiento efectivo que reduzca la necesidad de toma de medicamentos y permita tener bajo control los síntomas de aquellos pacientes que refieren desórdenes funcionales de colon, entre los que se encuentra el síndrome de intestino irritable.
El objetivo de este estudio era identificar pacientes con SGNC entre aquellos que informaron de una mejora de sus síntomas gastrointestinales mientras mantenían una dieta sin gluten (DSG) a lo largo de una provocación con gluten controlada por placebo de doble ciego con cruce. El estudio se realizó en 15 centros externos gastrointestinales de Italia. Se incluyeron 140 pacientes adultos que acudieron de forma rutinaria a clínicas externas de gastroenterología y que cumplían los criterios de Roma III en lo que respecta a los desórdenes funcionales gastrointestinales. Todos estaban siguiendo una dieta con gluten y daban negativo para IgA anti tTG y para IgE provocada por alergia al trigo y tenían valores normales de IgA total. A aquellos pacientes con una sospecha más elevada de enfermedad celíaca se les realizó una biopsia duodenal para descartar casos de enfermedad celíaca con serología negativa.
La fase 1 del estudio fue investigar la respuesta de los sujetos a una DSG. Se evaluaron los síntomas y la calidad de vida utilizando una serie de escalas visuales análogas (EVA) de 10 cm y un cuestionario SF36. Después de esta evaluación inicial, se les pidió a los pacientes que mantuvieran una DSG durante 3 semanas. Un nutricionista experto proporcionó información detallada y ofreció ayuda a los pacientes para todo lo relacionado con la dieta. Al final de la fase 1, los pacientes repitieron la EVA y el cuestionario SF36. Solo se consideró que «respondían ante el gluten» aquellos pacientes que indicaron una mejora significativa en su bienestar (EVA ≥ 3 cm, n=101); y a estos se les incluyó en la fase 2 del estudio.
A los pacientes que respondieron ante el gluten se les solicitó que mantuviesen su DSG estricta durante la fase 2 del estudio (provocación con gluten controlada por placebo doble ciego cruzado). En esta fase del estudio estaban incluidos 98 sujetos donde 3 de ellos se negaron a completar la prueba debido al miedo de que los síntomas reapareciesen durante la provocación con gluten. Los pacientes se seleccionaron aleatoriamente para recibir o bien cápsulas de gluten purificado (5,6 g/día, equivalente a 80 g de pasta seca) o la misma cantidad de cápsulas placebo (almidón de arroz) durante 7 días. Se estableció una suspensión de 7 días entre los periodos de cruce, por lo que la duración total de la fase 2 ascendió a 21 días (los pacientes siguieron una dieta sin gluten durante todos ellos). Al final de cada periodo de 7 días (provocación con gluten/placebo, suspensión y cruce) los sujetos rellenaron las EVA y el cuestionario SF36. En general los pacientes indicaron un mayor empeoramiento de su bienestar durante la ingesta de gluten que durante la administración del placebo (p=0,05). 28 de los pacientes aleatorizados se identificaron como «positivos» a la provocación con gluten controlada por placebo doble ciego cruzado (es decir, con una recaída sintomática durante la ingesta de gluten) y 69 se consideraron «negativos» (es decir, sin ninguna reacción sintomática durante la administración de gluten). No se encontró ningún factor demográfico, clínico o bioquímico que se pudiera asociar con la respuesta al gluten. Entre los pacientes positivos no parece haber un efecto significativo de la secuencia de cápsulas. De forma notable, 14 de los 28 pacientes también se consideraron como que respondían ante el placebo indicando, tal y como se esperaba, solo por el significativo «efecto placebo».
En total, el 14 % de los 98 pacientes aleatorizados que «respondían al gluten» mostraron una recaída sintomática durante la ingesta de gluten controlada por placebo doble ciego (sin respuesta simultánea al placebo) y, consecuentemente, pueden definirse como pacientes con SGNC. Este hallazgo confirma que la ingesta de gluten puede provocar síntomas gastrointestinales en un subgrupo de pacientes con desórdenes funcionales de intestino. Este estudio es el primero en valorar el comportamiento de los criterios de diagnóstico de los expertos de Salerno 1 para la SGNC en un entorno clínico. El gran número de pacientes que respondieron a una DSG (75 %) pero que dieron negativo a la ingesta de gluten es interesante, ya que se puede imputar un posible efecto placebo a cierta parte de esta discrepancia, pero también puede ser que muchos pacientes sean sensibles a otros componentes no específicos del trigo como, por ejemplo, ATI’s o FODMAP’s.
Leer artículo completo
1 Catassi C, Elli L, Bonaz B et al. Diagnosis of Non-coeliac Gluten Sensitivity (NCGS): The Salerno Experts Criteria. Nutrients 2015; 7: 4966-4977.

Una prueba de orina ayuda a controlar la dieta sin gluten
El único tratamiento eficaz para la enfermedad celíaca
hasta el momento, es seguir una dieta estricta sin gluten durante toda la vida. Sin embargo según cuentan los pacientes, por diversos motivos, el cumplimiento de la dieta no les resulta fácil y hasta un tercio de ellos comete transgresiones tanto voluntarias como involuntarias.
Hasta el momento se conocen al menos dos conflictos a la hora de realizar es seguimiento de la adherencia a la dieta:
1.-No hay consenso en cuanto a la frecuencia óptima de
el control en los pacientes
2.- Los análisis serológicos son insuficientemente sensibles para
detectar transgresiones ocasionales
3.- La única prueba para comprobar si existe lesión en el intestino es la biopsia, y es una prueba invasiva muy costosa y muy molesta para el paciente.
La orina tiene ventajas únicas para el muestreo como
menor su coste, ser una prueba no invasiva, de fácil recolección, transporte y almacenamiento.
El objetivo del estudio por tanto se vio alcanzado al superar los retos técnicos y mostrar la viabilidad de la medición de gluten péptidos inmunogénicos en la orina.
Para más información les recomendamos leer el artículo completo

La introducción del gluten en la dieta del lactante: recomendaciones de un grupo de expertos
El momento idóneo para la introducción del gluten en la dieta del lactante ha sido y continúa siendo motivo de controversia. Durante años ha prevalecido la recomendación del Comité de Nutrición de la Sociedad Europea de Gastroenterología, Hepatología y Nutrición (ESPGHAN) de evitar tanto su introducción precoz, antes de los 4 meses, como la tardía, después de los 7 meses, y de introducirlo gradualmente mientras el niño recibe lactancia materna. Se pretendía así reducir el riesgo de desarrollar enfermedad celíaca, alergia al gluten y diabetes. Sin embargo, dos estudios independientes publicados a finales de 2014 llegaron a la conclusión de que ni la edad de la introducción del gluten modifica el riesgo de desarrollar enfermedad celíaca, ni la lactancia materna confiere protección frente a la misma.
En este contexto, un grupo de pediatras expertos en nutrición y gastroenterología infantil ha elaborado un documento de consenso basado en las evidencias científicas actuales, en el que establece unas recomendaciones generales para la introducción del gluten en la dieta del lactante.
>>>Leer texto completo<<<
Fuente: AEP (asociación Española de Pediatría)

Implicación de la IL-33/ST2 en el proceso inflamatorio de los celíacos
>>>Leer artículo completo<<<

Revisión sistemática con metaanálisis: la alimentación infantil precoz y la enfermedad celíaca, actualización de 2015
La lactancia materna y la EC
El estudio PREVENT CD mostró que la lactancia materna, exclusiva o no, no influía significativamente en el desarrollo de la EC. Por otro lado, el CELIPREV reveló que la duración del periodo de lactancia era similar en los niños que desarrollaban EC como en los que no la desarrollaban. No obstante, ninguno de estos estudios estaba diseñado de forma específica para investigar sobre el papel de la lactancia materna en el desarrollo de la EC. Los resultados combinados de 5 estudios observacionales confirmaron estas conclusiones, y entre dichos estudios se vio una heterogeneidad considerable.
La lactancia materna en el momento de la introducción del gluten y la EC
Ni el estudio PREVENT CD ni el CELIPREV evidenciaron que estar con lactancia materna en el momento de la introducción del gluten influyera en el riesgo de desarrollar EC. Los resultados combinados de 7 estudios observacionales confirmaron estas conclusiones, y entre dichos estudios se vio una heterogeneidad considerable.
El momento de introducción del gluten en la dieta y la EC
El estudio PREVENT CD evidenció que la introducción del gluten a las 16 semanas en vez de a las 24 semanas, no reducía el riesgo de EC a los 3 años de edad. Por otro lado, en el estudio CELIPREV se observó que con la introducción del gluten a los 6 meses (en comparación con la introducción a los 12 meses) aumentaba el riesgo de EC a los 2 años, pero no a los 5 años (primeros resultados). Entre los diferentes estudios observacionales, no se encontraron diferencias significativas entre la introducción precoz y tardía del gluten en lo relativo al riesgo de padecer EC, a excepción del estudio ETICS. Este último estudio evidenció un aumento significativo del riesgo de padecer EC entre los niños en los que se había introducido el gluten a los 6 meses frente a aquellos en los que se había introducido el gluten en pequeñas cantidades entre los 4 y los 6 meses. Se vio una heterogeneidad considerable entre dichos estudios.
La cantidad de gluten durante el destete y la EC
El estudio PREVENT CD mostró que la ingesta media diaria de gluten no estaba relacionada con el desarrollo de EC, si bien, sólo se contaba con los resultados relativos a un subgrupo de participantes, pues esta variable no estaba contemplada como objetivo del estudio, y no se podían hacer comparaciones entre los grupos. Solamente en un estudio observacional se analizaron las cantidades de gluten que consumían los niños. Los resultados, indicaron que en los niños menores de 2 años, el riesgo de EC era mayor cuando se introducía el gluten en grandes cantidades frente a cantidades medianas o pequeñas. No obstante, las cantidades no se midieron en gramos por día y no se produjo ningún efecto en otros niños.
El tipo de alimentos con gluten y la EC
Se han realizado estudios no intervencionistas para evaluar el efecto del tipo de alimentos con gluten ingeridos sobre el riesgo de desarrollar EC. Los alimentos se clasificaron como “alimentos sólidos” (pan, galletas, papilla, pasta) o preparados de continuación con gluten, y los resultados indicaron que el tipo de alimento suministrado no constituía un factor de riesgo independiente para desarrollar EC.
El gluten durante la lactancia materna y la EC
El estudio PREVENT CD mostró que la dieta de la madre durante el embarazo y la lactancia no producía ningún efecto sobre el riesgo de desarrollar EC por parte del hijo.
Los autores de esta revisión concluyeron que el momento de introducción del gluten y la duración o continuación de la lactancia en el momento de introducción del gluten, no influyen en el riesgo de padecer EC (al menos durante los periodos estudiados). Sin embargo, los datos relativos a la cantidad de gluten ingerido durante el destete y el riesgo de desarrollar EC no son concluyentes. Existen pocos datos sobre el tipo de alimentos con gluten consumido durante el destete y el riesgo de padecer EC, pero no parece que sea un factor de riesgo. No se han encontrado estudios diseñados para evaluar el efecto de las prácticas de alimentación sobre el riesgo de padecer EC en niños con diferentes tipos de HLA. La alta prevalencia de EC en los niños de corta edad homocigotos para HLA 2.5, parece indicar que en caso de que las prácticas de alimentación jugaran algún papel, éste sería secundario en los niños con alta predisposición genética. Esta revisión sistemática actualizada no confirma la evidencia previa (derivada de estudios observacionales) que apuntaba a la edad en la introducción del gluten y la influencia del destete, sobre el riesgo de desarrollar EC. Por tanto, es necesario actualizar las recomendaciones europeas en esta materia.
Resource: Aliment Pharmacol and Ther 2015; 41 1038-105

Non-celiac gluten sensitivity has narrowed the spectrum of irritable bowel syndrome: A double-blind randomized placebo-controlled trial
148 adult patients with IBS and fulfilling the Rome III criteria were initially recruited from a private gastroenterology clinic in Tehran. Patients excluded from the study included those with a diagnosis of coeliac disease or inflammatory bowel disease, those who were already following or had previously followed a wheat or gluten free diet, those using drugs for depression/ anxiety, those using non-steroidal anti-inflammatory drugs, and those with abnormal electrolytes levels or thyroid function tests. The resulting patient sample eligible to commence a gluten free diet was 102, of these 22 patients withdrew from the study on the basis that the diet was too difficult to follow. A further 8 patients found relief from a gluten free diet but decided to withdraw as they were unprepared to follow the diet strictly. The remaining 72 patients completed the study (19 males and 53 females). Patients were randomly assigned to the gluten group (35 patients; 6 males and 29 females; mean age 44.5 +/- 10 years) or the placebo group (37 patients; 13 males and 24 females; mean age 43.2 +/- 17 years). There was no statistical difference between the 2 groups in terms of IBS sub-type. Patients completed a visual analogue symptom questionnaire at baseline to investigate primary outcomes including bloating, abdominal pain, defecation satisfaction, nausea, fatigue, and overall symptoms. Serum markers were measured for IgA anti-tTG, IgA anti-gliadin and IgG anti-gliadin antibodies, HLA typing was also performed for all patients.
All 72 patients then commenced a 6 week gluten free diet with weekly assessment by a dietitian to monitor and support compliance. After 6 weeks the gluten group were each asked to consume 100g/day (2 x 50g doses) of gluten powder (FODMAP free), the placebo group were asked to consume 100g/ day of gluten-free powder (rice flour, corn starch and glucose). Powders were mixed with warm water and consumed with breakfast and tea each day for a further 6 weeks. All patients remained on a gluten free diet for this second 6 week phase of the study.
After the 6 week challenge phase, symptoms were controlled in 25.7% of the gluten-containing group v’s 83.8% in the placebo group, indicating that 26 of the 35 patients in the gluten group became symptomatic on gluten challenge. Symptoms increased significantly in the gluten group, particularly for bloating and abdominal pain within 1 week of commencing the gluten challenge. No statistical difference was noted in serum antibody levels after gluten challenge. The authors of this study conclude that there is growing evidence that gastrointestinal symptoms in many IBS patients may be improved after gluten exclusion and differentiation between patients with IBS responsive to FODMAP restriction and those with Non-coeliac gluten sensitivity is important. This is particularly the case since evidence is emerging that a low FODMAP diet may reduce numbers of favourable bacteria in the gut (1,2). The authors went on to suggest a potential algorithm for the management of IBS patients fulfilling Rome III criteria that first implements a 6 week gluten free diet and goes on to recommend further carbohydrate restriction only in non-responders.
1. Staudacher HM, Lomer MC, Anderson JL et al. Fermentable carbohydrate restriction reduces luminal bifidobacteria and gastrointestinal symptoms in patients with irritable bowel syndrome. J Nutr 2012; 142: 1510-1518
2. Halmos EP, Christopherson CT, Bird AR et al. Diet that differ in their FODMAP content alter the colonic luminal microenvironment. Gut 2015; 64:93-100
Resource: Nutrients June 2015; 7:4542-4554
Shahbazkhani B, Sadeghi A, Malekzadeh R et al

Diagnosis of Non-Celiac Gluten Sensitivity (NCGS): The Salerno Experts’ Criteria
Non-Celiac Gluten Sensitivity (NCGS) is a syndrome characterized by intestinal and extra-intestinal symptoms related to the ingestion of gluten-containing food, in subjects that are not affected by either celiac disease or wheat allergy. Given the lack of a NCGS biomarker, there is the need for standardizing the procedure leading to the diagnosis confirmation. In this paper we report experts’ recommendations on how the diagnostic protocol should be performed for the confirmation of NCGS. A full diagnostic procedure should assess the clinical response to the gluten-free diet (GFD) and measure the effect of a gluten challenge after a period of treatment with the GFD. The clinical evaluation is performed using a self-administered instrument incorporating a modified version of the Gastrointestinal Symptom Rating Scale. The patient identifies one to three main symptoms that are quantitatively assessed using a Numerical Rating Scale with a score ranging from 1 to 10. The double-blind placebo-controlled gluten challenge (8 g/day) includes a one-week challenge followed by a one-week washout of strict GFD and by the crossover to the second one-week challenge. The vehicle should contain cooked, homogeneously distributed gluten. At least a variation of 30% of one to three main symptoms between the gluten and the placebo challenge should be detected to discriminate a positive from a negative result. The guidelines provided in this paper will help the clinician to reach a firm and positive diagnosis of NCGS and facilitate the comparisons of different studies, if adopted internationally.
Resource: Nutrients 2015, 7(6), 4966-4977; doi:10.3390/nu7064966
Carlo Catassi, Luca Elli, Bruno Bonaz, Gerd Bouma, Antonio Carroccio, Gemma Castillejo, Christophe Cellier, Fernanda Cristofori, Laura de Magistris, Jernej Dolinsek, Walburga Dieterich, Ruggiero Francavilla, Marios Hadjivassiliou, Wolfgang Holtmeier, Ute Körner, Dan A. Leffler,Knut E. A. Lundin, Giuseppe Mazzarella, Chris J. Mulder, Nicoletta Pellegrini, Kamran Rostami, David Sanders, Gry Irene Skodje, Detlef Schuppan, Reiner Ullrich, Umberto Volta, Marianne Williams, Victor F. Zevallos, Yurdagül Zopf and Alessio Fasano

Small Amounts of Gluten in Subjects With Suspected Nonceliac Gluten Sensitivity: A Randomized, Double-Blind, Placebo-Controlled, Cross-Over Trial.
BACKGROUND & AIMS:
There is debate over the existence of nonceliac gluten sensitivity (NCGS) intestinal and extraintestinal symptoms in response to ingestion of gluten-containing foods by people without celiac disease or wheat allergy. We performed a randomized, double-blind, placebo-controlled, cross-over trial to determine the effects of administration of low doses of gluten to subjects with suspected NCGS.
METHODS:
We enrolled 61 adults without celiac disease or a wheat allergy who believed ingestion of gluten-containing food to be the cause of their intestinal and extraintestinal symptoms. Participants were assigned randomly to groups given either 4.375 g/day gluten or rice starch (placebo) for 1 week, each via gastrosoluble capsules. After a 1-week gluten-free diet, participants crossed over to the other group. The primary outcome was the change in overall (intestinal and extraintestinal) symptoms, determined by established scoring systems, between gluten and placebo intake. A secondary outcome was the change in individual symptom scores between gluten vs placebo.
RESULTS:
According to the per-protocol analysis of data from the 59 patients who completed the trial, intake of gluten significantly increased overall symptoms compared with placebo (P = .034). Abdominal bloating (P = .040) and pain (P = .047), among the intestinal symptoms, and foggy mind (P = .019), depression (P = .020), and aphthous stomatitis (P = .025), among the extraintestinal symptoms, were significantly more severe when subjects received gluten than placebo.
CONCLUSIONS:
In a cross-over trial of subjects with suspected NCGS, the severity of overall symptoms increased significantly during 1 week of intake of small amounts of gluten, compared with placebo.
Resource: Clin Gastroenterol Hepatol. 2015 Sep;13(9):1604-1612.
Di Sabatino A, Volta U, Salvatore C, Biancheri P, Caio G, De Giorgio R, Di Stefano M, Corazza GR.

Clinical effectiveness and economic costs of group versus one-to-one education for short-chain fermentable carbohydrate restriction (low FODMAP diet) in the management of irritable bowel syndrome.
Patients were considered suitable for inclusion if they had been diagnosed with IBS by their primary care physician or gastroenterologist using NICE criteria, had organic disease ruled out and had been referred for dietetic advice. These patients were first offered a telephone consultation which lasted up to 15 minutes during which they were assessed for suitability to join a group session (brief assessment including symptoms, medical history and dietary intake). Those considered suitable were given a group appointment. Patients considered unsuitable for group education included those with atypical symptoms, complex health issues or language barriers, these patients were offered one-to-one dietetic appointments. Symptom type and severity, alongside stool frequency and form were assessed at base-line and at follow up by means of a questionnaire. Patients who did not attend follow-up were excluded from the study. Patients attending group sessions also completed additional questionnaires to assess the acceptability of group education.
The initial appointment for group sessions lasted approximately 90 minutes and included up to 12 patients. One-to-one sessions lasted approximately 1 hour. Follow up appointments (booked a minimum of 6 weeks later) were delivered using the same educational approach as at baseline (group or one-to-one). Data from 263 patients attending group sessions was compared to data from 101 patients attending one-to-one education. There was no significant difference between groups for IBS subtype at baseline. There was a significant increase in the proportion of patients reporting ‘yes’ to the global symptom question (‘do you currently have satisfactory relief of your gut symptoms’) following low FODMAP advice via both methods of education (18% at baseline versus 54% at follow-up for group education, and 5% at baseline versus 60% at follow-up for one-to-one education), with no difference at follow-up between the 2 methods. Patients had a significant decrease in composite symptom score following low FODMAP dietary advice, composite scores were not significantly different between the two methods of education at follow-up.
At follow-up, 93% of patients reported adherence to the diet at least 50% of the time. The majority of patients (87%) reported that the written information provided was easy to understand and 49% found the diet easy to follow. Following group education, 36% of patients would have preferred one-to-one education, with the remainder preferring group education (22%) or expressing no preference (42%). Most (81%) felt that group education had provided sufficient information to manage their symptoms without further advice. Unfortunately, non-attendance data was not reported in this study as the primary focus was symptom response (requiring those who did not attend follow up to be excluded from the evaluation). The cost of providing low FODMAP dietary advice was calculated as £67.19 per patient for group education (assuming 12 patients per group) and £139.20 per patient for one-to-one education. The cost of a QALY gain for this group pathway was well below the £20,000 to £30,000 threshold for UK healthcare costs.
In conclusion, this study shows that dietitian-led FODMAP group education is clinically effective and the costs associated with a FODMAP group pathway are worthy of further investigation.
Resource: Journal of Human Nutrition and Dietetics (2015). 10.1111/jhn.12318
Whigham L, Joyce T, Harper G et al

Systematic review: non coeliac gluten sensitivity
Non coeliac gluten sensitivity (NCGS) is a controversial emerging disorder. Despite reported symptoms related to the ingestion of gluten, NCGS remains a diagnosis based on the exclusion of coeliac disease, given the absence of reliable biomarkers.
Aim
To evaluate the prevalence, diagnostic exclusion of coeliac disease and the efficacy of a gluten-free diet (GFD) for NCGS patients.
Methods
A PubMed search was performed up to December 2014. According to consensus diagnostic criteria, NCGS was defined as self-reported gluten intolerance, negative coeliac serology and absence of villous atrophy. Studies evaluating the impact of a GFD on patients with irritable bowel syndrome (IBS) were also included.
Results
Prevalence rates of NCGS (0.5–13%) differed widely. Seventeen studies, including 1561 patients (26 children), met the inclusion criteria for NCGS. HLA haplotypes could not be linked to histology [normal or lymphocytic enteritis (LE)] in 1123 NCGS patients. HLADQ2/DQ8 haplotypes were present in 44% of NCGS patients. After advanced diagnostic techniques in 189 NCGS patients combining LE and HLADQ2/DQ8 haplotypes, 39 (20%) were reclassified as coeliac disease. There was a higher than expected family history of coeliac disease and autoimmune disorders in NCGS patients. A GFD resulted in variable results for variable, but significantly improved stool frequency in HLADQ2 positive diarrhoea-predominant IBS patients.
Conclusions
Prevalence rates for NCGS are extremely variable. A subset of NCGS patients might belong in the so-called ‘coeliac-lite’ disease. The benefit of a GFD for NCGS patients is currently controversial. HLADQ2 positive diarrhoea- type IBS patients might gain symptom improvement from a GFD.
Resource: Aliment Pharmacol Ther. 2015 May;41(9):807-20. doi: 10.1111/apt.13155. Epub 2015 Mar 6.
Molina-Infante J, Santolaria S, Sanders DS, Fernández-Bañares F.

A Study Evaluating the Bidirectional Relationship Between Inflammatory Bowel Disease and Self-reported Non-coeliac Gluten Sensitivity.
No significant difference was found between patients with ulcerative colitis and Crohn’s disease in terms of prevalence on SR-NCGS and gluten free diet usage. However, IBD patients with SR-NCGS were significantly more likely to have stricturing disease (p=0.046) and more active disease (p=0.002) as measured by the Crohn’s Disease Activity Index score. This indicates that the presence of SR-NCGS may be a marker for clinicians of underlying severe/ structuring disease. The mechanism for the potential therapeutic effect of a gluten free diet in IBD is not well understood. The volume/ physical properties and ‘higher residue’ nature of gluten-containing foods may lead patients to avoid such products. It is also possible that an unidentified immunological mechanism may contribute to the relief experienced by patients choosing to reduce or eliminate their intake of gluten. The absence of diagnostic markers for NCGS mean it is unclear whether individuals with IBD who self-report gluten sensitivity are sensitive the gluten or other components of wheat such as mannans, amylase-trypsin inhibitors or FODMAPs. Further studies are needed to understand whether a gluten-free diet, or indeed a wider wheat free diet may be a valuable dietetic intervention in selected patients with IBD.
Resource: Inflammatory Bowel Disease 2015 Feb 24 epub ahead of print.
Aziz A, Branchi F, Pearson K, Priest J, Sanders D.
Association between Coeliac Disease and Psoriasis: Italian Primary Care Multicentre Study
Coeliac disease is increasingly associated with extraintestinal manifestations, among these, several skin disorders have been reported, with dermatitis herpetiformis being the best recognised. Several studies investigating the possible association between CD and psoriasis have been published, however results have so far proven to be inconclusive and most of the data on the effect of a gluten free diet on psoriatic skin lesions are contained within case reports.
In this prospective multicentre study, the patient records from 19 Italian primary care practices were screened for confirmed cases of psoriasis, following this 219 patients with a confirmed diagnosis of psoriasis were enrolled in to the study (111 males, 51%; mean age 54 years), and 264 age and sex matched controls without psoriasis. The severity of psoriasis amongst subjects was assessed at base-line and follow up, in addition to gastrointestinal symptoms. Serum levels of anti-tTG were recorded for all subjects and if positive, CD diagnosis was confirmed by histology on biopsy. A total of 49% of the 218 enrolled patients with psoriasis reported one or more GI symptom, the most common being heartburn/ acid regurgitation (27%) and bloating (16%). Nine out of 218 patients with psoriasis showed positive serology for CD compared to only 1 out of the 264 controls (P=<0.05). Histology confirmed the CD diagnosis in all subjects with positivity to anti-tTG antibodies. All patients with psoriasis and CD adhered to a gluten free diet and completed the 6 month follow up. At 3 months, all 9 patients showed significant improvement in the severity of their psoriasis, this improvement was maintained at 6 months in all but 1 patient whose symptoms worsened.
This study shows a significant epidemiological association between CD and psoriasis in the Italian population. However, the small number of psoriatic patients with evidence of CD cannot be considered as definitive evidence of a causal link between the two disorders. The authors of this study hypothesise that the presence of shared genes (at-risk HLA haplotypes) often used to explain the greater prevalence of CD in several autoimmune disorders, might be present in subjects affected by psoriasis. In addition, CD-related malabsorption may affect psoriasis by causing a vitamin D deficiency status. It is well known that low levels of vitamin D pre-dispose to psoriasis, and that expose to sunlight and topical vitamin D preparations improve psoriatic lesions. Furthermore, an abnormal intestinal permeability common in untreated CD may increase the passage of different immune triggers. The fact that the majority of psoriatic subjects with positive CD serology showed complete villous atrophy is concordant with the hypotheses of vitamin D malabsorption and altered intestinal permeability to the passage of immune triggers.
Resource: Dermatology 2015 Feb 3.

Coeliac Disease in Women With Infertility - A Meta-Analysis
Although this study makes a case for screening women with infertility for coeliac disease. The authors acknowledge that their work alone cannot be used to prove a causal relationship between coeliac disease and infertility due to the limitation of the study design of case control studies, the small number of studies available overall and the small sample sizes used within these. A recent large population-based study of infertility and coeliac disease in UK women suggested that women with coeliac disease (both before and after diagnosis) do not have a greater chance of clinically recorded fertility problems than women without coeliac disease*. However, the design of this study has it's own limitations due to reliance on primary care records, the known mis-diagnosis of coeliac disease and delay in recording this within medical records.
Resource: Dhalwani N.N, West J et al (2014) Women with celiac disease present with fertility problems no more often than women in the general population. Gastroenterology 147: 1267-74

¿Es el gluten el gran agente etiopatogenico de enfermedad en el siglo XXI?
Introducción:
El gluten es una glucoproteína presente en algunos cereales. La incidencia de trastornos relacionados con el gluten está aumentando.
Objetivos:
Revisar la literatura científica sobre la patogenia de diferentes enfermedades y la posible relación de éstas con la ingesta de gluten, en pacientes no celiacos, no sensibles al gluten y sin alergia al trigo.
Métodos:
Búsqueda bibliográfica en las principales bases de datos científicas.
Resultados:
Se obtuvo información/resultados de las siguientes enfermedades: ataxia por gluten, esclerosis múltiple, trastorno del espectro autista, esquizofrenia, trastorno por déficit de atención con hiperactividad, trastornos depresivos, cefaleas, síndrome del intestino irritable, fibromialgia, dermatitis herpetiforme y epilepsia, en los que se hacía referencia a una determinación de antigliadina, o bien a la aplicación de un tratamiento con/sin gluten y se evaluaba la eficacia de la intervención.
Conclusión:
La ingesta de gluten parece estar relacionada con algunas enfermedades, incluso excluyendo a los pacientes que padezcan celiaquía, sensibilidad al gluten o alergia al trigo. Las sospechas, en dichas enfermedades, sobre el beneficio, como tratamiento complementario,de una dieta sin gluten, se han confirmando con ensayos semi-clínicos y cohortes, ya sea actuando sobre la patogenia, o como medida de mejora de la sintomatología. Son necesarios más estudios para confirmar una causa-efecto del gluten sobre estas patologías.
Resource: Nutr Hosp. 2014;30(6):1203-1210
Ismael San Mauro Martín, Elena Garicano Vilar, Luis Collado Yurrutia y María José Ciudad Cabañas

Glycaemic index of some commercial gluten-free foods
Purpose
Gluten-free products present major challenges for the food industry in terms of organoleptic, technological and nutritional characteristics. The absence of gluten has been shown to affect starch digestibility, thus increasing the postprandial glycaemic response. However, in recent years, gluten-free technologies have been improved, thus possibly modifying this quality parameter. We investigated the glycaemic index (GI) of 10 commercial foods aiming to update the GI values of the most common gluten-free products consumed in Italy.
Methods
The in vivo GI was evaluated for six bakery products and four types of pasta. The postprandial glucose response was obtained in two groups with 10 healthy volunteers each.
Results
The overall GI values ranged from 37.5 for breakfast biscuits to 66.7 for puffed multigrain cake. Breads and pasta had GI values consistently lower than those previously reported in the literature.
Conclusion
The present study showed that several commercial GF products exhibited low and medium GI values, not confirming the previous observations on the high GI of GF. However, considering the multiple formulations and processes for preparation of these products, further studies are recommended.
Resource: Eur J Nutr. 2014 Oct 17.
Francesca Scazzina • Margherita Dall’Asta • Nicoletta Pellegrini • Furio Brighenti
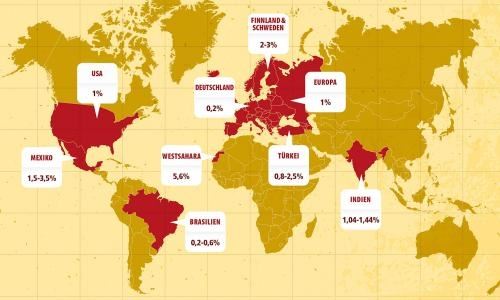
The New Epidemiology of Celiac Disease
The prevalence of celiac disease (CD) varies greatly, but several reports have shown that CD is increasing in frequency in different geographic areas. The increase in prevalence can be partially attributed to the improvement in diagnostic techniques and disease awareness; however the equally well documented rise in incidence in the last 30–40 years cannot be so easily explained. The new epidemiology of CD is now characterized by an increase of new cases in the historical CD areas (northern Europe and the United States) and more interestingly in a spread of the disease in new regions (Asian countries). A significant change in diet habits, particularly in gluten consumption as well as in infant feeding patterns are probably the main factors that can account for these new trends in CD epidemiology.
Resource: Journal of Pediatric Gastroenterology & Nutrition, July 2014 Volume 59

Enfermedad celíaca: diez cosas que todo experto en nutrición y gastroenterología debe saber
Aquí tiene un resumen de los 10 puntos
Hay 10 cosas que todos los expertos en nutrición y gastroenterología deberían saber sobre la enfermedad celíaca.
(1) El análisis de transglutaminasa tisular de inmunoglobulina A es la mejor prueba serológica para detectar la enfermedad celíaca.
(2) La enfermedad celíaca puede determinarse por medio de una endoscopia aún así, una apariencia endoscópica normal no descarta el diagnóstico.
(3) Se recomienda que se extraigan 4 biopsias del segundo tramo del duodeno y 2 biopsias del bulbo, de las posiciones de las 9 y las 12 en punto para maximizar la sensibilidad y poder obtener confirmación histológica de enfermedad celíaca.
(4) Plantéese realizar pruebas serológicas a parientes de primer grado, pacientes con diabetes mellitus tipo 1, con síndrome de Down, de Turner y de Williams, así como a aquellos con osteoporosis prematura, déficit de hierro, bioquímicas anormales de hígado y otras manifestaciones de la enfermedad celíaca.
(5) A los pacientes que ya lleven tiempo con una dieta sin gluten deberían hacérseles pruebas para detectar la presencia de HLA DQ2 o DQ8, evitando de esa forma la necesidad de otras evaluaciones para la enfermedad celíaca en portadores no alélicos.
(6) El tratamiento básico de esta enfermedad es una dieta estricta sin gluten de por vida prescrita por un dietista experto. Todos aquellos pacientes que padezcan enfermedad celíaca deberían ser derivados a un dietista con amplia experiencia en esta enfermedad. En la actualidad existen directrices que indican que los dietistas deberían asesorar a pacientes con celiaquía. Si se deja que investiguen por su cuenta sobre la dieta sin gluten, los pacientes podrían encontrar información no veraz que podría derivar en un consumo innecesariamente restrictivo. Otras cuestiones prácticas abordadas por los dietistas son: cómo evitar la contaminación cruzada en casa (por ejemplo, tostadoras o recipientes separados) y consejos para viajar y comer fuera de casa También, es necesario revisar la salud general de un paciente que sigue una dieta sin gluten, ya que cada vez son más comunes la obesidad, la diabetes y otras co-morbilidades.
(7) En el caso de los adultos a los que se les ha diagnosticado recientemente la enfermedad celíaca deberían comprobarse las deficiencias de micronutrientes (hierro, B12, folatos, zinc, cobre), deficiencias de vitaminas liposolubles (vitamina D) y densitometría ósea.
(8) Todos los pacientes diagnosticados deberían tener un seguimiento clínico para garantizar la respuesta y la adhesión a la dieta sin gluten.
(9) En aquellos con síntomas persistentes o con recidivas debería revisarse la solidez del diagnóstico inicial, buscar la exposición al gluten y llevar a cabo una evaluación sistemática de enfermedades alternativas o asociadas.
(10) Deben realizarse evaluaciones a aquellos con una enfermedad refractaria por si hay evolución maligna.
Resource: Clin Gastroenterol Hepatol. 2014 Jul 19. pii: S1542-3565(14)01053-2

Early nutrition: prevention of celiac disease?
Celiac disease (CD) is an autoimmune disorder caused by ingestion of gluten in genetically predisposed individuals. It is a chronic, multiorgan disease in which small-intestinal mucosal damage may lead to malabsorption of nutrients. In the last years, several studies suggested a protective role of breast-feeding and/or the timing and quantity of gluten introduction in the subsequent development of CD. Especially, prolonged breast feeding during the introduction of gluten-containing feeding has been associated with a reduced risk of developing CD in infancy. The focus of this review was to present the actual knowledge of the possible preventive influence of early nutrition on the risk to develop CD.
Resource: J Pediatr Gastroenterol Nutr. 2014 Jul;59 Suppl 1:S18-20
Schaart MW, Mearin ML

Randomised clinical trial: Gluten may cause depression in subjects with non-coeliac gluten sensitivity – an exploratory clinical study
Background
Current evidence suggests that many patients with self-reported non-coeliac gluten sensitivity (NCGS) retain gastrointestinal symptoms on a gluten-free diet (GFD) but continue to restrict gluten as they report ‘feeling better’.
Aim
To investigate the notion that a major effect of gluten in those with NCGS is on mental state and not necessarily on gastrointestinal symptoms.
Methods
Twenty-two subjects (24–62 years, five male) with irritable bowel syndrome who had coeliac disease excluded but were symptomatically controlled on a GFD, undertook a double-blind cross-over study. Participants randomly received one of three dietary challenges for 3 days, followed by a minimum 3-day washout before crossing over to the next diet. Challenge gluten-free food was supplemented with gluten (16 g/day), whey (16 g/day) or not supplemented (placebo). End-points included mental state as assessed by the Spielberger State Trait Personality Inventory (STPI), cortisol secretion and gastrointestinal symptoms.
Results
Gluten ingestion was associated with higher overall STPI state depression scores compared to placebo [M = 2.03, 95% CI (0.55–3.51), P = 0.010] but not whey [M = 1.48, 95% CI (−0.14 to 3.10), P = 0.07]. No differences were found for other STPI state indices or for any STPI trait measures. No difference in cortisol secretion was identified between challenges. Gastrointestinal symptoms were induced similarly across all dietary challenges.
Conclusions
Short-term exposure to gluten specifically induced current feelings of depression with no effect on other indices or on emotional disposition. Gluten-specific induction of gastrointestinal symptoms was not identified. Such findings might explain why patients with non-coeliac gluten sensitivity feel better on a gluten-free diet despite the continuation of gastrointestinal symptoms.
Resource: Alimentary Pharmacology & Therapeutics, Volume 39, Issue 10, pages 1104–1112, May 2014
S. L. Peters, J. R. Biesiekierski, G. W. Yelland, J. G. Muir1 and P. R. Gibson

Celiac Disease or Non-Celiac Gluten Sensitivity? An Approach to Clinical Differential Diagnosis
OBJECTIVES: Differentiating between celiac disease (CD) and non-celiac gluten sensitivity (NCGS) is important for appropriate management but is often challenging.
METHODS: We retrospectively reviewed records from 238 patients who presented for the evaluation of symptoms responsive to gluten restriction without prior diagnosis or exclusion of CD. Demographics, presenting symptoms, serologic, genetic, and histologic data, nutrient deficiencies, personal history of autoimmune diseases, and family history of CD were recorded. NCGS was defined as symptoms responsive to a gluten-free diet (GFD) in the setting of negative celiac serology and duodenal biopsies while on a gluten-containing diet or negative human leukocyte antigen (HLA) DQ2/DQ8 testing.
RESULTS: Of the 238 study subjects, 101 had CD, 125 had NCGS, 9 had non-celiac enteropathy, and 3 had indeterminate diagnosis. CD subjects presented with symptoms of malabsorption 67.3% of the time compared with 24.8% of the NCGS subjects (P<0.0001). In addition, CD subjects were significantly more likely to have a family history of CD (P=0.004), personal history of autoimmune diseases (P=0.002), or nutrient deficiencies (P<0.0001). The positive likelihood ratio for diagnosis of CD of a >2× upper limit of normal IgA trans-glutaminase antibody (tTG) or IgA/IgG deaminated gliadan peptide antibody (DGP) with clinical response to GFD was 130 (confidence interval (CI): 18.5–918.3). The positive likelihood ratio of the combination of gluten-responsive symptoms and negative IgA tTG or IgA/IgG DGP on a regular diet for NCGS was 9.6 (CI: 5.5–16.9). When individuals with negative IgA tTG or IgA/IgG DGP also lacked symptoms of malabsorption (weight loss, diarrhea, and nutrient deficiencies) and CD risk factors (personal history of autoimmune diseases and family history of CD), the positive likelihood ratio for NCGS increased to 80.9.
CONCLUSIONS: On the basis of our findings, we have developed a diagnostic algorithm to differentiate CD from NCGS. Subjects with negative celiac serologies (IgA tTG or IgA/IgG DGP) on a regular diet are unlikely to have CD. Those with negative serology who also lack clinical evidence of malabsorption and CD risk factors are highly likely to have NCGS and may not require further testing. Those with equivocal serology should undergo HLA typing to determine the need for biopsy.
Resource: The American Journal of Gastroenterology 109, 741-746 (May 2014)
Toufic A Kabbani, Rohini R Vanga, Daniel A Leffler, Javier Villafuerte-Galvez, Kumar Pallav, Joshua Hansen, Rupa Mukherjee, Melinda Dennis and Ciaran P Kelly

Characterization of Adults With a Self-Diagnosis of Nonceliac Gluten Sensitivity
Background: Nonceliac gluten sensitivity (NCGS), occurring in patients without celiac disease yet whose gastrointestinal symptoms improve on a gluten-free diet (GFD), is largely a self-reported diagnosis and would appear to be very common. The aims of this study were to characterize patients who believe they have NCGS.
Materials and Methods: Advertising was directed toward adults who believed they had NCGS and were willing to participate in a clinical trial. Respondents were asked to complete a questionnaire about symptoms, diet, and celiac investigation.
Results: Of 248 respondents, 147 completed the survey. Mean age was 43.5 years, and 130 were women. Seventy-two percent did not meet the description of NCGS due to inadequate exclusion of celiac disease (62%), uncontrolled symptoms despite gluten restriction (24%), and not following a GFD (27%), alone or in combination. The GFD was self-initiated in 44% of respondents; in other respondents it was prescribed by alternative health professionals (21%), dietitians (19%), and general practitioners (16%). No celiac investigations had been performed in 15% of respondents. Of 75 respondents who had duodenal biopsies, 29% had no or inadequate gluten intake at the time of endoscopy. Inadequate celiac investigation was common if the GFD was initiated by self (69%), alternative health professionals (70%), general practitioners (46%), or dietitians (43%). In 40 respondents who fulfilled the criteria for NCGS, their knowledge of and adherence to the GFD were excellent, and 65% identified other food intolerances.
Conclusions: Just over 1 in 4 respondents self-reporting as NCGS fulfill criteria for its diagnosis. Initiation of a GFD without adequate exclusion of celiac disease is common. In 1 of 4 respondents, symptoms are poorly controlled despite gluten avoidance.
Resource: Nutr Clin Pract April 16, 2014
Jessica R. Biesiekierski, PhD, RN, Evan D. Newnham , MD, FRACP, Susan J. Shepherd, PhD, APD, Jane G. Muir, PhD, APD, Peter R. Gibson, MD, FRACP

Usefulness of Symptoms to Screen for Celiac Disease
OBJECTIVE:
To describe the frequency of symptoms and associated conditions among screening-detected celiac disease (CD) cases and non-CD children and to evaluate questionnaire-based case-finding targeting the general population.
METHODS:
In a population-based CD screening of 12-year-olds, children and their parents completed questionnaires on CD-associated symptoms and conditions before knowledge of CD status. Questionnaire data for those who had their CD detected in the screening (n = 153) were compared with those of children with normal levels of CD markers (n = 7016). Hypothetical case-finding strategies were also evaluated. Questionnaires were returned by 7054 (98%) of the children and by 6294 (88%) of their parents.
RESULTS:
Symptoms were as common among screening-detected CD cases as among non-CD children. The frequency of children with screening-detected CD was similar when comparing the groups with and without any CD-related symptoms (2.1% vs 2.1%; P = .930) or CD-associated conditions (3.6% vs 2.1%; P = .07). Case-finding by asking for CD-associated symptoms and/or conditions would have identified 52 cases (38% of all cases) at a cost of analyzing blood samples for 2282 children (37%) in the study population.
CONCLUSIONS:
The current recommended guidelines for finding undiagnosed CD cases, so-called active case-finding, fail to identify the majority of previously undiagnosed cases if applied in the general population of Swedish 12-year-olds. Our results warrant further studies on the effectiveness of CD case-finding in the pediatric population, both at the clinical and population-based levels.
Resource: Pediatrics. 2014 Feb;133(2):211-8. doi: 10.1542/peds.2012-3765. Epub 2014 Jan 13

Daño celular intestinal y respuesta inmune sistémica en individuos con sensibilidad al gluten no celíaca

Anemia en la enfermedad celíaca en edad pediátrica: asociación de características clínicas e histológicas y respuesta a una dieta libre de gluten

Eficacia de una dieta sin gluten en sujetos con síndrome del intestino irritable (SII) / diarrea predominante y que desconozcan su genotipo HLA-DQ2/8.

¿Es beneficiosa la dieta sin gluten en la esclerosis múltiple?

Diagnóstico de sensibilidad al gluten no celiaca en pacientes con síntomas gastrointestinales funcionales

Una prueba de orina ayuda a controlar la dieta sin gluten

La introducción del gluten en la dieta del lactante: recomendaciones de un grupo de expertos

Implicación de la IL-33/ST2 en el proceso inflamatorio de los celíacos

Revisión sistemática con metaanálisis: la alimentación infantil precoz y la enfermedad celíaca, actualización de 2015

Non-celiac gluten sensitivity has narrowed the spectrum of irritable bowel syndrome: A double-blind randomized placebo-controlled trial

Diagnosis of Non-Celiac Gluten Sensitivity (NCGS): The Salerno Experts’ Criteria

Small Amounts of Gluten in Subjects With Suspected Nonceliac Gluten Sensitivity: A Randomized, Double-Blind, Placebo-Controlled, Cross-Over Trial.

Clinical effectiveness and economic costs of group versus one-to-one education for short-chain fermentable carbohydrate restriction (low FODMAP diet) in the management of irritable bowel syndrome.

Systematic review: non coeliac gluten sensitivity

A Study Evaluating the Bidirectional Relationship Between Inflammatory Bowel Disease and Self-reported Non-coeliac Gluten Sensitivity.

Association between Coeliac Disease and Psoriasis: Italian Primary Care Multicentre Study

Coeliac Disease in Women With Infertility - A Meta-Analysis

¿Es el gluten el gran agente etiopatogenico de enfermedad en el siglo XXI?

Glycaemic index of some commercial gluten-free foods

The New Epidemiology of Celiac Disease

Enfermedad celíaca: diez cosas que todo experto en nutrición y gastroenterología debe saber

Early nutrition: prevention of celiac disease?

Randomised clinical trial: Gluten may cause depression in subjects with non-coeliac gluten sensitivity – an exploratory clinical study

Celiac Disease or Non-Celiac Gluten Sensitivity? An Approach to Clinical Differential Diagnosis

Characterization of Adults With a Self-Diagnosis of Nonceliac Gluten Sensitivity

