Comorbilidades de la enfermedad celíaca

Con una prevalencia del 13,8 %, las enfermedades autoinmunes afectan mucho más a menudo a los pacientes celíacos que al resto de la población. No sólo ocurre con las enfermedades autoinmunes, la enfermedad celíaca también se asocia a intolerancias alimentarias, enfermedades genéticas, endocrinas y neurológicas.
A menudo la enfermedad celíaca puede ir acompañada de otras enfermedades autoinmunes ya que se asocia a un mayor riesgo de sufrir distintas enfermedades. Entre las enfermedades autoinmunes cabe destacar la diabetes tipo 1, pero al mismo tiempo, con frecuencia se dan enfermedades hepáticas y tiroideas en combinación con la enfermedad celíaca. En cuanto a otras enfermedades asociadas cabe mencionar, la dermatitis herpetiforme o de Duhring, una enfermedad inflamatoria de la piel, que se conoce como la manifestación cutánea de la enfermedad celíaca. Por otro lado, debido a la inflamación y atrofia vellositaria, antes del diagnóstico y durante el periodo inicial tras este, los pacientes celíacos pueden desarrollar una intolerancia secundaria a la lactosa. También se habla de un mayor riesgo a padecer osteoporosis y problemas de fertilidad debidos principalmente a problemas de malabsorción.
Diabetes tipo 1
La enfermedad celíaca y la diabetes tipo 1 a menudo aparecen juntas. La prevalencia de la enfermedad celíaca en los pacientes diabéticos tipo 1 varía según la edad del paciente, pero suele rondar entre el 3-7 % de los afectados. La enfermedad celíaca también aparece a menudo en los parientes de primer grado de un diabético. Si estudiamos el dato a la inversa, observamos que también en este caso, entre el 3 y el 6 % de los pacientes celíacos padecen diabetes tipo 1.
Características comunes genéticas
La aparición conjunta de ambas enfermedades parece ser causada por una predisposición genética común, ya que tanto en la diabetes como en la enfermedad celíaca se observa una frecuencia mayor de los denominados genes de histocompatibilidad HLA-DQ2 y HLA-DQ8. Asimismo, tanto en los diabéticos de tipo 1 como en los pacientes celíacos se han constatado niveles de zonulina elevados, siendo esta una proteína que regula la permeabilidad del intestino delgado.
Diagnóstico de la diabetes
En la mayoría de los casos (cerca del 90 %) se diagnostica la diabetes tipo 1 antes que la enfermedad celíaca. Esto probablemente se debe a que la enfermedad celíaca presenta pocos síntomas en los pacientes afectados durante la infancia y la juventud. Cabe destacar que cuanto más tarde se diagnostique la enfermedad celíaca y cuanto más tiempo se consuman alimentos con gluten, más riesgo hay de padecer diabetes.
Recomendaciones alimentarias
Cuando se sufren estas dos enfermedades, se debe seguir una alimentación estricta sin gluten, pero ninguna alimentación específica para diabéticos. Hoy en día se recomienda que los diabéticos, tanto si padecen enfermedad celíaca como si no, sigan una alimentación normal y equilibrada, controlando individualizadamente la toma de hidratos de carbono. En este sentido, la alimentación sin gluten tiene efectos positivos en la diabetes, puesto que la absorción, y por tanto el metabolismo del enfermo, está mejor controlado y con ello, es posible reducir la necesidad de insulina.
Cribado de la enfermedad celíaca en diabéticos tipo 1
Ante la frecuente asociación de estas dos patologías, todos los diabéticos tipo 1 deberían ser sometidos a un cribado para enfermedad celíaca, en el que se determina la presencia de los anticuerpos tTg-IgA:
Características comunes genéticas
La aparición conjunta de ambas enfermedades parece ser causada por una predisposición genética común, ya que tanto en la diabetes como en la enfermedad celíaca se observa una frecuencia mayor de los denominados genes de histocompatibilidad HLA-DQ2 y HLA-DQ8. Asimismo, tanto en los diabéticos de tipo 1 como en los pacientes celíacos se han constatado niveles de zonulina elevados, siendo esta una proteína que regula la permeabilidad del intestino delgado.
Diagnóstico de la diabetes
En la mayoría de los casos (cerca del 90 %) se diagnostica la diabetes tipo 1 antes que la enfermedad celíaca. Esto probablemente se debe a que la enfermedad celíaca presenta pocos síntomas en los pacientes afectados durante la infancia y la juventud. Cabe destacar que cuanto más tarde se diagnostique la enfermedad celíaca y cuanto más tiempo se consuman alimentos con gluten, más riesgo hay de padecer diabetes.
Recomendaciones alimentarias
Cuando se sufren estas dos enfermedades, se debe seguir una alimentación estricta sin gluten, pero ninguna alimentación específica para diabéticos. Hoy en día se recomienda que los diabéticos, tanto si padecen enfermedad celíaca como si no, sigan una alimentación normal y equilibrada, controlando individualizadamente la toma de hidratos de carbono. En este sentido, la alimentación sin gluten tiene efectos positivos en la diabetes, puesto que la absorción, y por tanto el metabolismo del enfermo, está mejor controlado y con ello, es posible reducir la necesidad de insulina.
Cribado de la enfermedad celíaca en diabéticos tipo 1
Ante la frecuente asociación de estas dos patologías, todos los diabéticos tipo 1 deberían ser sometidos a un cribado para enfermedad celíaca, en el que se determina la presencia de los anticuerpos tTg-IgA:
- En el momento del diagnóstico de la diabetes
- Durante los primeros tres años, una vez al año
- Cinco años después del diagnóstico de la diabetes
- Si existen síntomas sospechosos
Tiroiditis de Hashimoto
Aparte de la diabetes tipo 1, a menudo se asocian a la enfermedad celíaca de manera desproporcionada enfermedades tiroideas autoinmunes, especialmente la tiroiditis de Hashimoto, con una prevalencia del 3 al 10 %. Esta particularidad, se da especialmente en los pacientes diagnosticados en la edad adulta, coincidiendo con que la tiroiditis autoinmune es la causa más común de hipotiroidismo en la edad adulta. Esta enfermedad se manifiesta a través de una destrucción parcial o total del tejido de la tiroides, que se ve debilitado por los autoanticuerpos.
Detectar a tiempo las enfermedades tiroideas
Dado que realizar un cribado es relativamente sencillo y las enfermedades tiroideas no se manifiestan con síntomas unívocos, los pacientes celíacos deberían revisarse la hormona estimulante de la tiroides (TSH) en el momento del diagnóstico de la enfermedad celíaca y, posteriormente de forma periódica durante varios años. Esta recomendación se extiende los parientes de primer grado de pacientes con enfermedad celíaca y/o enfermedades tiroideas autoinmunes.
Terapia para pacientes celíacos
Cuando exista un hipotiroidismo funcional, puede indicarse una terapia con preparados a base de LT4. En los pacientes celíacos recién diagnosticados, se debería ajustar la dosis del preparado, ya que debido a la atrofia vellositaria que sufren los enfermos, la absorción y asimilación de la LT4 y del resto de medicamentos necesarios puede verse reducida. Tras seguir una temporada una dieta estricta sin gluten, la mucosa del intestino delgado puede volver a regenerarse por completo, de manera que las dosis necesarias deben volver a ajustarse en consecuencia.
Detectar a tiempo las enfermedades tiroideas
Dado que realizar un cribado es relativamente sencillo y las enfermedades tiroideas no se manifiestan con síntomas unívocos, los pacientes celíacos deberían revisarse la hormona estimulante de la tiroides (TSH) en el momento del diagnóstico de la enfermedad celíaca y, posteriormente de forma periódica durante varios años. Esta recomendación se extiende los parientes de primer grado de pacientes con enfermedad celíaca y/o enfermedades tiroideas autoinmunes.
Terapia para pacientes celíacos
Cuando exista un hipotiroidismo funcional, puede indicarse una terapia con preparados a base de LT4. En los pacientes celíacos recién diagnosticados, se debería ajustar la dosis del preparado, ya que debido a la atrofia vellositaria que sufren los enfermos, la absorción y asimilación de la LT4 y del resto de medicamentos necesarios puede verse reducida. Tras seguir una temporada una dieta estricta sin gluten, la mucosa del intestino delgado puede volver a regenerarse por completo, de manera que las dosis necesarias deben volver a ajustarse en consecuencia.
Hepatitis autoinmune
La hepatitis autoinmune es una enfermedad autoinmune inflamatoria crónica o aguda del hígado poco común. El propio sistema inmunitario debilita las células hepáticas, lo que da lugar a la inflamación del hígado (hepatitis). A raíz del trasfondo genético global, a menudo una hepatitis autoinmune se presenta en combinación con la enfermedad celíaca. Al mismo tiempo, la asociación entre estas dos enfermedades autoinmunes aumenta proporcionalmente con la edad del paciente en el momento del diagnóstico. En el 30 % de los pacientes mayores de 20 años, además de la enfermedad celíaca se manifiesta también una enfermedad autoinmune.
Detectar las enfermedades hepáticas a tiempo
Dado que realizar un cribado es relativamente sencillo y las enfermedades hepáticas no se manifiestan con síntomas unívocos, los pacientes celíacos deberían someterse a pruebas de la función hepática en el momento del diagnóstico de la enfermedad celíaca y, posteriormente de forma periódica durante varios años.
Detectar las enfermedades hepáticas a tiempo
Dado que realizar un cribado es relativamente sencillo y las enfermedades hepáticas no se manifiestan con síntomas unívocos, los pacientes celíacos deberían someterse a pruebas de la función hepática en el momento del diagnóstico de la enfermedad celíaca y, posteriormente de forma periódica durante varios años.
Intolerancia a la lactosa
A raíz de la atrofia vellositaria, antes del diagnóstico y durante el periodo inicial tras este, los pacientes celíacos pueden desarrollar una intolerancia secundaria a la lactosa. Las lesiones de la mucosa del intestino delgado pueden causar una deficiencia de lactasa, de modo que el disacárido lactosa ya no se hidroliza ni se absorbe por completo. Debido a esto, al principio estos pacientes deberían seguir una alimentación no solo sin gluten, sino también sin lactosa. En la fase de remisión, el afectado normalmente puede volver a tolerar la lactosa.
Deficiencia de lactasa persistente
En algunos casos la intolerancia a la lactosa puede persistir incluso después de haber empezado la dieta sin gluten y a pesar de que la mucosa del intestino delgado se haya regenerado. Esto se atribuye a una deficiencia genética de la enzima, que es bastante común en la población del sur de Europa y que es independiente a la enfermedad celíaca. Se estima que en España cerca del 40% de la población tiene intolerancia a la lactosa.
Deficiencia de lactasa persistente
En algunos casos la intolerancia a la lactosa puede persistir incluso después de haber empezado la dieta sin gluten y a pesar de que la mucosa del intestino delgado se haya regenerado. Esto se atribuye a una deficiencia genética de la enzima, que es bastante común en la población del sur de Europa y que es independiente a la enfermedad celíaca. Se estima que en España cerca del 40% de la población tiene intolerancia a la lactosa.
Dermatitis herpetiforme (DH)
La dermatitis herpetiforme Duhring (DH) es una enfermedad cutánea inflamatoria caracterizada por la aparición de una erupción cutánea con pápulas que produce una fuerte picazón y que suele ser de color rojo. Debido al fuerte picor, los afectados se rascan a menudo, de modo que se forman costras. En el 90 % de los pacientes, la erupción cutánea aparece en los codos y antebrazos. Otras zonas a menudo afectadas son el trasero y la parte delantera de la rodilla. La DH prácticamente solo afecta a los sujetos con piel clara, y la incidencia ascienda a aprox. 1:10 000.
Relación con la enfermedad celíaca
La DH se considera la manifestación cutánea de la enfermedad celíaca, si se diagnostica DH a un paciente, se asume automáticamente que este también sufre enfermedad celíaca. Sin embargo, no sucede necesariamente lo mismo a la inversa. En muchos pacientes con DH los síntomas de la enfermedad celíaca son muy débiles y generalmente no se detecta hasta que aparece la típica erupción cutánea. La DH se diagnostica a través de un examen cutáneo y del diagnóstico clásico de la enfermedad celíaca (prueba de anticuerpos y biopsia del intestino delgado).
Causas genéticas
La enfermedad se describió por primera vez como entidad clínica en 1884 y recibe el nombre de su descubridor: L. A. Duhring. No obstante, el hecho de que existe una relación entre la DH y la enfermedad celíaca no se constató hasta finales de los años 60, cuando en estudios familiares se observó que los parientes de pacientes afectados con DH a menudo también desarrollaban una DH o padecían enfermedad celíaca. Los estudios han demostrado que en ambas enfermedades están implicados los mismos genes. Nuestro cuerpo cuenta con los denominados antígenos HLA, que controlan la reacción inmunitaria, y en la DH y la enfermedad celíaca, se observan los genotipos HLA DR3-DQ2 y DR3-DQ8. Estos antígenos son indispensables para el desarrollo de cualquiera de las dos enfermedades mencionadas.
Terapia de la DH
Tanto la DH como la enfermedad celíaca responden al consumo de gluten negativamente. Por ello, como en el caso de la enfermedad celíaca, el seguimiento de una alimentación sin gluten estricta representa el único tratamiento eficaz para la DH. Sin embargo, en la mayoría de los pacientes pasa mucho tiempo hasta que la alimentación sin gluten hace que desaparezcan los síntomas de la DH. Por ello, entretanto además de la dieta sin gluten, se requiere un tratamiento con medicamentos con el que la erupción cutánea desaparece en el plazo de una semana. Aun así, la erupción cutánea solo desaparecerá a largo plazo si se sigue una alimentación estricta sin gluten. Las dosis de los medicamentos no pueden reducirse hasta seis y ocho meses después del diagnóstico, pero normalmente después de dos años es posible eliminar por completo la medicación y seguir sólo con la dieta sin gluten.
Relación con la enfermedad celíaca
La DH se considera la manifestación cutánea de la enfermedad celíaca, si se diagnostica DH a un paciente, se asume automáticamente que este también sufre enfermedad celíaca. Sin embargo, no sucede necesariamente lo mismo a la inversa. En muchos pacientes con DH los síntomas de la enfermedad celíaca son muy débiles y generalmente no se detecta hasta que aparece la típica erupción cutánea. La DH se diagnostica a través de un examen cutáneo y del diagnóstico clásico de la enfermedad celíaca (prueba de anticuerpos y biopsia del intestino delgado).
Causas genéticas
La enfermedad se describió por primera vez como entidad clínica en 1884 y recibe el nombre de su descubridor: L. A. Duhring. No obstante, el hecho de que existe una relación entre la DH y la enfermedad celíaca no se constató hasta finales de los años 60, cuando en estudios familiares se observó que los parientes de pacientes afectados con DH a menudo también desarrollaban una DH o padecían enfermedad celíaca. Los estudios han demostrado que en ambas enfermedades están implicados los mismos genes. Nuestro cuerpo cuenta con los denominados antígenos HLA, que controlan la reacción inmunitaria, y en la DH y la enfermedad celíaca, se observan los genotipos HLA DR3-DQ2 y DR3-DQ8. Estos antígenos son indispensables para el desarrollo de cualquiera de las dos enfermedades mencionadas.
Terapia de la DH
Tanto la DH como la enfermedad celíaca responden al consumo de gluten negativamente. Por ello, como en el caso de la enfermedad celíaca, el seguimiento de una alimentación sin gluten estricta representa el único tratamiento eficaz para la DH. Sin embargo, en la mayoría de los pacientes pasa mucho tiempo hasta que la alimentación sin gluten hace que desaparezcan los síntomas de la DH. Por ello, entretanto además de la dieta sin gluten, se requiere un tratamiento con medicamentos con el que la erupción cutánea desaparece en el plazo de una semana. Aun así, la erupción cutánea solo desaparecerá a largo plazo si se sigue una alimentación estricta sin gluten. Las dosis de los medicamentos no pueden reducirse hasta seis y ocho meses después del diagnóstico, pero normalmente después de dos años es posible eliminar por completo la medicación y seguir sólo con la dieta sin gluten.
Osteoporosis
Tras varios estudios, se ha observado un mayor riesgo de fracturas en los sujetos que sufren enfermedad celíaca en comparación con la población sana. En la mayoría de los casos esto se atribuye a una densitometría ósea baja, lo que hace pensar que el mayor riesgo de fracturas observado a menudo está relacionado con los sujetos con una enfermedad celíaca no tratada que no mantienen una alimentación estricta sin gluten. Además, de la enfermedad celíaca, otros factores también tienen efectos en la densitometría ósea y en consecuencia, en el riesgo de fracturas. La determinación de la densitometría ósea solo es aconsejable en pacientes que ya siguen una dieta sin gluten y que presentan otros factores de riesgo aparte de la enfermedad celíaca.
Aparición de tumores malignos
El riesgo de desarrollar un tumor maligno en el caso de los pacientes celíacos es ligeramente mayor en comparación con el resto de la población. Se dan con mayor frecuencia tumores malignos específicos, en la región del esófago o el intestino delgado. Para reducir este riesgo, es muy importante seguir una alimentación sin gluten, ya que puede proteger de la aparición de tumores malignos asociados con la enfermedad celíaca.
Abortos de repetición
La enfermedad celíaca no diagnosticada o no tratada en las mujeres puede dar lugar a abortos de repetición y complicaciones en el embarazo, es decir, dificultades para gestar, partos prematuros o abortos, y también puede tener efectos negativos en el peso del recién nacido. Todavía no se ha aclarado si puede deberse simplemente a una malabsorción de determinadas sustancias nutritivas causada por la atrofia vellositaria, o bien si entran en juego factores inmunológicos.
Otras comorbilidades de la enfermedad celíaca
- Falta de lgA selectiva
- Síndrome de Sjögren
- Cirrosis biliar primaria
- Enfermedad de Crohn
- Síndrome de Down
- Síndrome de Turner
- Síndrome de Williams
- Epilepsia
Más información sobre este tema...
Presentación
1
Mostrar todo
Estudios
2
Mostrar todo

Gluten and Gut-Brain Axis: Lesson Learned From Autism And Schizophrenia (2015)
Alessio Fasano, M.D.
Mucosal Immunology and Biology Research Center
Center for Celiac Research
Massachusetts General Hospital for Children
16th International Coeliac Disease Symposium 2015 a Praga
Pre-Conference Workshop on Gluten Sensitivity "The Evolving Planet of Gluten Related Disorders"
Mucosal Immunology and Biology Research Center
Center for Celiac Research
Massachusetts General Hospital for Children
16th International Coeliac Disease Symposium 2015 a Praga
Pre-Conference Workshop on Gluten Sensitivity "The Evolving Planet of Gluten Related Disorders"

Gluten and Gut-Brain Axis: Lesson Learned From Autism And Schizophrenia (2015)
Alessio Fasano, M.D.
Mucosal Immunology and Biology Research Center
...
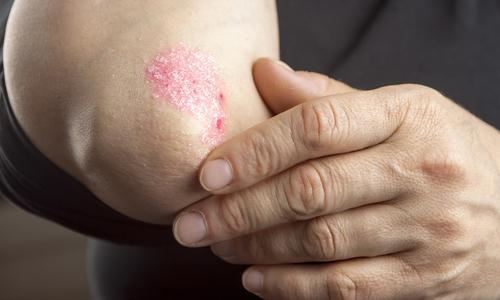
Association between Coeliac Disease and Psoriasis: Italian Primary Care Multicentre Study
Summary
Coeliac disease is increasingly associated with extraintestinal manifestations, among these, several skin disorders have been reported, with dermatitis herpetiformis being the best recognised. Several studies investigating the possible association between CD and psoriasis have been published, however results have so far proven to be inconclusive and most of the data on the effect of a gluten free diet on psoriatic skin lesions are contained within case reports.
In this prospective multicentre study, the patient records from 19 Italian primary care practices were screened for confirmed cases of psoriasis, following this 219 patients with a confirmed diagnosis of psoriasis were enrolled in to the study (111 males, 51%; mean age 54 years), and 264 age and sex matched controls without psoriasis. The severity of psoriasis amongst subjects was assessed at base-line and follow up, in addition to gastrointestinal symptoms. Serum levels of anti-tTG were recorded for all subjects and if positive, CD diagnosis was confirmed by histology on biopsy. A total of 49% of the 218 enrolled patients with psoriasis reported one or more GI symptom, the most common being heartburn/ acid regurgitation (27%) and bloating (16%). Nine out of 218 patients with psoriasis showed positive serology for CD compared to only 1 out of the 264 controls (P=<0.05). Histology confirmed the CD diagnosis in all subjects with positivity to anti-tTG antibodies. All patients with psoriasis and CD adhered to a gluten free diet and completed the 6 month follow up. At 3 months, all 9 patients showed significant improvement in the severity of their psoriasis, this improvement was maintained at 6 months in all but 1 patient whose symptoms worsened.
This study shows a significant epidemiological association between CD and psoriasis in the Italian population. However, the small number of psoriatic patients with evidence of CD cannot be considered as definitive evidence of a causal link between the two disorders. The authors of this study hypothesise that the presence of shared genes (at-risk HLA haplotypes) often used to explain the greater prevalence of CD in several autoimmune disorders, might be present in subjects affected by psoriasis. In addition, CD-related malabsorption may affect psoriasis by causing a vitamin D deficiency status. It is well known that low levels of vitamin D pre-dispose to psoriasis, and that expose to sunlight and topical vitamin D preparations improve psoriatic lesions. Furthermore, an abnormal intestinal permeability common in untreated CD may increase the passage of different immune triggers. The fact that the majority of psoriatic subjects with positive CD serology showed complete villous atrophy is concordant with the hypotheses of vitamin D malabsorption and altered intestinal permeability to the passage of immune triggers.
Resource: Dermatology 2015 Feb 3.
Coeliac disease is increasingly associated with extraintestinal manifestations, among these, several skin disorders have been reported, with dermatitis herpetiformis being the best recognised. Several studies investigating the possible association between CD and psoriasis have been published, however results have so far proven to be inconclusive and most of the data on the effect of a gluten free diet on psoriatic skin lesions are contained within case reports.
In this prospective multicentre study, the patient records from 19 Italian primary care practices were screened for confirmed cases of psoriasis, following this 219 patients with a confirmed diagnosis of psoriasis were enrolled in to the study (111 males, 51%; mean age 54 years), and 264 age and sex matched controls without psoriasis. The severity of psoriasis amongst subjects was assessed at base-line and follow up, in addition to gastrointestinal symptoms. Serum levels of anti-tTG were recorded for all subjects and if positive, CD diagnosis was confirmed by histology on biopsy. A total of 49% of the 218 enrolled patients with psoriasis reported one or more GI symptom, the most common being heartburn/ acid regurgitation (27%) and bloating (16%). Nine out of 218 patients with psoriasis showed positive serology for CD compared to only 1 out of the 264 controls (P=<0.05). Histology confirmed the CD diagnosis in all subjects with positivity to anti-tTG antibodies. All patients with psoriasis and CD adhered to a gluten free diet and completed the 6 month follow up. At 3 months, all 9 patients showed significant improvement in the severity of their psoriasis, this improvement was maintained at 6 months in all but 1 patient whose symptoms worsened.
This study shows a significant epidemiological association between CD and psoriasis in the Italian population. However, the small number of psoriatic patients with evidence of CD cannot be considered as definitive evidence of a causal link between the two disorders. The authors of this study hypothesise that the presence of shared genes (at-risk HLA haplotypes) often used to explain the greater prevalence of CD in several autoimmune disorders, might be present in subjects affected by psoriasis. In addition, CD-related malabsorption may affect psoriasis by causing a vitamin D deficiency status. It is well known that low levels of vitamin D pre-dispose to psoriasis, and that expose to sunlight and topical vitamin D preparations improve psoriatic lesions. Furthermore, an abnormal intestinal permeability common in untreated CD may increase the passage of different immune triggers. The fact that the majority of psoriatic subjects with positive CD serology showed complete villous atrophy is concordant with the hypotheses of vitamin D malabsorption and altered intestinal permeability to the passage of immune triggers.
Resource: Dermatology 2015 Feb 3.

Coeliac Disease in Women With Infertility - A Meta-Analysis
The first indications of a link between female infertility and coeliac disease was first described over 40 years ago. However, contemporary studies have failed to reach a consensus on whether patients with infertility should be screened for coeliac disease. Many studies on this subject are small, are of poor design and/ or lack a control arm. This latest meta-analysis on the subject sought to assess whether women with infertility are at higher risk of coeliac disease. Studies excluded from the meta-analysis included those without control data, those where diagnosis of coeliac disease was based only on serology, and studies where exact data regarding the number of patients included was unavailable. 105 studies were identified as a result of the initial literature search, of these only 16 were suitable for study in detail, 11 of which did not meet the inclusion criteria, leaving just 5 for inclusion in the meta-analysis to calculate the odds of having coeliac disease in women with all cause infertility and unexplained infertility. Four further studies that had been excluded on the basis that they lacked a control arm were included for calculation of the pooled prevalence of coeliac disease in women with infertility. Studies that reported coeliac disease diagnosis based on serology but with incomplete biopsy data were all included for the calculation of pooled serological prevalence of CD in women with infertility (12 studies). The meta-analysis showed that women with infertility had a 3.5 times increased odds of having coeliac disease in comparison with that in the control population. Of 422 women with unexplained infertility across the five included studies, 14 were found to have coeliac disease, representing a 6 fold increase in the odds of having coeliac disease in comparison to the control group. When data from studies without a control arm were analysed, pooled prevalence of coeliac disease amongst 884 women with all cause infertility and 623 women with unexplained infertility was 2.3% and 3.2%, respectively. Pooled serological prevalence of coeliac disease amongst women with all-cause infertility and unexplained infertility was 1.3% and 3.1%, respectively. Micronutrient deficiencies have been suggested as a possible mechanism for infertility amongst women with coeliac disease. In this meta-analysis, 28.5% of infertility patients with coeliac disease had iron deficiency in the 4 studies that reported iron status. Among the 4 studies that reported folic acid status, none of the patients with infertility and coeliac disease were deficient in this nutrient.
Although this study makes a case for screening women with infertility for coeliac disease. The authors acknowledge that their work alone cannot be used to prove a causal relationship between coeliac disease and infertility due to the limitation of the study design of case control studies, the small number of studies available overall and the small sample sizes used within these. A recent large population-based study of infertility and coeliac disease in UK women suggested that women with coeliac disease (both before and after diagnosis) do not have a greater chance of clinically recorded fertility problems than women without coeliac disease*. However, the design of this study has it's own limitations due to reliance on primary care records, the known mis-diagnosis of coeliac disease and delay in recording this within medical records.
Resource: Dhalwani N.N, West J et al (2014) Women with celiac disease present with fertility problems no more often than women in the general population. Gastroenterology 147: 1267-74
Although this study makes a case for screening women with infertility for coeliac disease. The authors acknowledge that their work alone cannot be used to prove a causal relationship between coeliac disease and infertility due to the limitation of the study design of case control studies, the small number of studies available overall and the small sample sizes used within these. A recent large population-based study of infertility and coeliac disease in UK women suggested that women with coeliac disease (both before and after diagnosis) do not have a greater chance of clinically recorded fertility problems than women without coeliac disease*. However, the design of this study has it's own limitations due to reliance on primary care records, the known mis-diagnosis of coeliac disease and delay in recording this within medical records.
Resource: Dhalwani N.N, West J et al (2014) Women with celiac disease present with fertility problems no more often than women in the general population. Gastroenterology 147: 1267-74

Association between Coeliac Disease and Psoriasis: Italian Primary Care Multicentre Study
Summary
Coeliac disease is increasingly associated with extraintest...

Coeliac Disease in Women With Infertility - A Meta-Analysis
The first indications of a link between female infertility and coeliac...
www.drschaer-institute.com
