Pathologies associées à la maladie cœliaque

Contrairement aux personnes en bonne santé, les personnes souffrant de la maladie cœliaque présentent assez fréquemment des maladies auto-immunes (prévalence de 13,8 %) mais également des intolérances et des maladies génétiques, endocriniennes et neurologiques.
La maladie cœliaque s’accompagne souvent de maladies auto-immunes ainsi que de pathologies diverses associées. En tête des maladies auto-immunes, on classe le diabète de type 1, mais également assez souvent des maladies du foie et de la thyroïde. Parmi les maladies associées, on trouve par exemple la dermatite herpétiforme de Dühring. C’est du reste la manifestation cutanée spécifique de la maladie cœliaque. Avant, et même peu après, que le diagnostic ne soit posé, les personnes souffrant de la maladie cœliaque peuvent aussi être victimes d’une intolérance secondaire au lactose. Le risque accru d'ostéoporose ainsi que les troubles de la fertilité associés à la maladie cœliaque font l’objet de débat.
Diabète de type 1
La maladie cœliaque et le diabète de type 1 apparaissent fréquemment de façon concomitante. La prévalence de la maladie cœliaque chez les diabétiques de type 1 se situe, selon l'âge des patients, entre 3 et 8 %. En ce qui concerne les parents du premier degré d’un diabétique, on remarque assez fréquemment des cas de maladie cœliaque. À l’inverse, 3 à 6 % des personnes souffrant de la maladie cœliaque souffre du diabète de type 1.
Similitudes génétiques
À l’origine de l'apparition simultanée des deux maladies, il semble y avoir une prédisposition génétique commune : on remarque tant chez les diabétiques que chez les personnes souffrant de la maladie cœliaque une augmentation des gènes d‘histocompatibilité HLA-DQ2 et HLA-DQ8. En outre, on a remarqué chez ces mêmes patients un taux de zonuline accru. La zonuline est une protéine qui règle la perméabilité des muqueuses de l'intestin grêle.
Diagnostic du diabète
Dans la plupart des cas (environ 90 %), le diagnostic du diabète de type 1 est d'abord posé. Cela tient probablement au fait que les symptômes de la maladie cœliaque sont assez peu marqués dans la petite enfance et l‘adolescence des patients concernés. Les personnes dont la maladie cœliaque n'a pas été diagnostiquée à temps et qui continuent d’avoir une alimentation riche en gluten présente un risque plus élevé d’avoir du diabète.
Recommandations concernant l'alimentation
Pour traiter les deux maladies, il n’est pas nécessaire de consommer des produits alimentaires dits « pour diabétiques », il faut observer en revanche un régime strict sans gluten. À l’heure actuelle, on recommande aux diabétiques, qu’ils souffrent ou non de la maladie cœliaque, une alimentation normale et équilibrée. L'alimentation sans gluten a aussi des effets bénéfiques sur le diabète puisque l’on peut, une fois le métabolisme mieux contrôlé, envisager une éventuelle réduction des prises d‘insuline.
Dépistage de la maladie cœliaque chez les diabétiques de type 1
Au vu de l'association fréquente des deux pathologies, tous les diabétiques de type 1 devraient être soumis à un dépistage de la maladie cœliaque, assorti d’un dosage des anticorps tTg-IgA:
Similitudes génétiques
À l’origine de l'apparition simultanée des deux maladies, il semble y avoir une prédisposition génétique commune : on remarque tant chez les diabétiques que chez les personnes souffrant de la maladie cœliaque une augmentation des gènes d‘histocompatibilité HLA-DQ2 et HLA-DQ8. En outre, on a remarqué chez ces mêmes patients un taux de zonuline accru. La zonuline est une protéine qui règle la perméabilité des muqueuses de l'intestin grêle.
Diagnostic du diabète
Dans la plupart des cas (environ 90 %), le diagnostic du diabète de type 1 est d'abord posé. Cela tient probablement au fait que les symptômes de la maladie cœliaque sont assez peu marqués dans la petite enfance et l‘adolescence des patients concernés. Les personnes dont la maladie cœliaque n'a pas été diagnostiquée à temps et qui continuent d’avoir une alimentation riche en gluten présente un risque plus élevé d’avoir du diabète.
Recommandations concernant l'alimentation
Pour traiter les deux maladies, il n’est pas nécessaire de consommer des produits alimentaires dits « pour diabétiques », il faut observer en revanche un régime strict sans gluten. À l’heure actuelle, on recommande aux diabétiques, qu’ils souffrent ou non de la maladie cœliaque, une alimentation normale et équilibrée. L'alimentation sans gluten a aussi des effets bénéfiques sur le diabète puisque l’on peut, une fois le métabolisme mieux contrôlé, envisager une éventuelle réduction des prises d‘insuline.
Dépistage de la maladie cœliaque chez les diabétiques de type 1
Au vu de l'association fréquente des deux pathologies, tous les diabétiques de type 1 devraient être soumis à un dépistage de la maladie cœliaque, assorti d’un dosage des anticorps tTg-IgA:
- Une fois le diagnostic du diabète posé
- Tous les ans durant trois ans
- Cinq ans après le diagnostic du diabète
- En cas de symptômes suspects
Thyroïdite de Hashimoto
À côté de diabète de type 1, des maladies auto-immunes de la thyroïde, la thyroïdite de Hashimoto est proportionnellement très fréquemment associée à la maladie cœliaque (prévalence de 3 à 10 %). Et ce, en particulier pour les patients qui ne sont diagnostiqués qu’à un âge avancé. La thyroïdite auto-immune est la cause la plus fréquente d'un hypothyréose à l'âge adulte. Elle s’accompagne d‘une destruction partielle ou complète du tissu thyroïdien.
Déceler à temps les maladies de la thyroïde
Dans la mesure où un dépistage est relativement facile à mettre en œuvre et que les maladies de la thyroïde ne se manifestent pas toujours par des symptômes évidents à reconnaître, les personnes souffrant de la maladie cœliaque devraient effectuer un dosage de l’hormone thyréostimulante (TSH) au moment où le diagnostic de la maladie cœliaque est posé ainsi qu’à intervalles réguliers pendant quelques années. Ces analyses sont recommandées aux parents du premier degré des patients souffrant de la maladie cœliaque, de maladies de la thyroïde ou de maladies auto-immunes.
Traitement des personnes souffrant de la maladie cœliaque
En cas d‘hypothyroïdie fonctionnelle, un traitement à base de levothyroxine (LT4) paraît tout indiqué. Pour les patients dont la laladie coeliaque a été récemment diagnostiquées, on pourra en raison de l’atrophie villositaire diminuer considérablement la prise de LT4 et envisager l’arrêt de tous les autres médicaments nécessaires. Il faudra absolument envisager une adaptation des doses prescrites. Dans le cadre d’un régime strict sans gluten, les muqueuses de l'intestin grêle peuvent encore se régénérer complètement de sorte que les doses nécessaires peuvent être réduites en conséquence.
Déceler à temps les maladies de la thyroïde
Dans la mesure où un dépistage est relativement facile à mettre en œuvre et que les maladies de la thyroïde ne se manifestent pas toujours par des symptômes évidents à reconnaître, les personnes souffrant de la maladie cœliaque devraient effectuer un dosage de l’hormone thyréostimulante (TSH) au moment où le diagnostic de la maladie cœliaque est posé ainsi qu’à intervalles réguliers pendant quelques années. Ces analyses sont recommandées aux parents du premier degré des patients souffrant de la maladie cœliaque, de maladies de la thyroïde ou de maladies auto-immunes.
Traitement des personnes souffrant de la maladie cœliaque
En cas d‘hypothyroïdie fonctionnelle, un traitement à base de levothyroxine (LT4) paraît tout indiqué. Pour les patients dont la laladie coeliaque a été récemment diagnostiquées, on pourra en raison de l’atrophie villositaire diminuer considérablement la prise de LT4 et envisager l’arrêt de tous les autres médicaments nécessaires. Il faudra absolument envisager une adaptation des doses prescrites. Dans le cadre d’un régime strict sans gluten, les muqueuses de l'intestin grêle peuvent encore se régénérer complètement de sorte que les doses nécessaires peuvent être réduites en conséquence.
Hépatite auto-immune
L'hépatite auto-immune est une maladie inflammatoire auto-immune rare, aiguë ou chronique du foie. Le système immunitaire s‘attaque aux cellules du foie provoquant une inflammation (hépatite). En raison du contexte génétique commun, une hépatite auto-immune se déclare fréquemment en association avec la maladie cœliaque. L'association de ces deux maladies auto-immunes est d'autant plus élevée que le diagnostic de la maladie cœliaque aura été posé tardivement. Parmi les 30 % des patients âgés de plus de 20 ans, on découvre une autre maladie auto-immune.
Déceler à temps les maladies du foie
Dans la mesure où un dépistage est relativement facile à mettre en œuvre et que les maladies du foie ne se manifestent pas toujours par des symptômes évidents à déceler, les personnes dont le diagnostic de la maladie cœliaque a été posé devraient effectuer des tests sur le fonctionnement du foie au moment du diagnostic puis régulièrement à quelques années d’intervalles.
Déceler à temps les maladies du foie
Dans la mesure où un dépistage est relativement facile à mettre en œuvre et que les maladies du foie ne se manifestent pas toujours par des symptômes évidents à déceler, les personnes dont le diagnostic de la maladie cœliaque a été posé devraient effectuer des tests sur le fonctionnement du foie au moment du diagnostic puis régulièrement à quelques années d’intervalles.
Intolérance au lactose
Compte tenu de l’atrophie des villosités, une intolérance secondaire au lactose peut se manifester avant même ou peu après la pose du diagnostic de la maladie cœliaque. L’altération des muqueuses de l'intestin grêle peut être à l’origine d’un déficit plus ou moins important en lactase de sorte que le lactose n’est plus complètement absorbé. Par conséquent, ces patients devraient adopter une alimentation non seulement sans gluten mais aussi, pour commencer, sans lactose. Dans la phase de rémission, les patients peuvent généralement à nouveau supporter le lactose.
Déficit en lactase permanent
Dans quelques cas, l’intolérance au lactose peut perdurer aussi après la mise en place d‘une alimentation sans gluten alors que les muqueuses de l’intestin grêle se sont régénérées. Cela est dû à un déficit génétique en lacatse qui apparaît dans les populations d'Europe méridionale, mais qui n’est toutefois pas déclenché par la maladie cœliaque. En France la prévalence du déficit primaire en Lactase croît du Nord (10-15%) au Sud (plus de 50%).
Déficit en lactase permanent
Dans quelques cas, l’intolérance au lactose peut perdurer aussi après la mise en place d‘une alimentation sans gluten alors que les muqueuses de l’intestin grêle se sont régénérées. Cela est dû à un déficit génétique en lacatse qui apparaît dans les populations d'Europe méridionale, mais qui n’est toutefois pas déclenché par la maladie cœliaque. En France la prévalence du déficit primaire en Lactase croît du Nord (10-15%) au Sud (plus de 50%).
Dermatite herpétiforme de Dühring
La dermatite herpétiforme de Dühring (DH) est une inflammation de la peau qui se traduit par la présence de papules érythémateuses groupées, de plaques d'urticaire rouges couronnées par des vésicules. La démangeaison chronique et les écorchures superficielles produites par le grattage entraînent l’apparition de croûte. 90 % des patients présentent ces lésions de la peau sur les coudes, les avant-bras, et, assez fréquemment sur le siège et le devant des genoux. La DH ne touche pratiquement que les personnes à peau claire. L'incidence s'élève à environ 1 sur 10.000.
Lien avec la maladie cœliaque
La DH est la manifestation cutanée spécifique de la maladie cœliaque. Un patient présentant une DH souffre de fait de la maladie cœliaque. L’inverse n’est pas nécessairement obligatoire. Chez un bon nombre de patients atteints de DH, la maladie cœliaque est si peu prononcée qu’elle passe le plus souvent inaperçue jusqu’au jour où l’éruption caractéristique apparaît. Le diagnostic de la DH se fait au moyen d’un test cutané et des méthodes classiques employées pour la maladie cœliaque (test anticorps + plus biopsie de l’intestin grêle).
Causes génétiques
La dermatite herpétiforme est dite de Dühring car c’est lui qui l’a décrite pour la première fois en 1884 comme constituant une entité clinique. En revanche son lien avec la maladie cœliaque n’a été découvert qu’à la fin des années 60. Dans les études effectuées sur les familles, on a constaté que les parents des personnes atteintes de DH développent souvent aussi une DH ou souffrent de la maladie cœliaque. Des études ont montré l’implication de gènes identiques dans les deux maladies.
Notre corps dispose de ce que l'on appelle les antigènes HLA qui déclenchent une réaction immunitaire. En cas de DH ou de maladie cœliaque, on a constaté la présence des génotypes HLA : DR3-DQ2 et DR3-DQ8. Ces antigènes prédisposent les personnes à développer une DH ou une maladie cœliaque.
Traitement de la DH
L’absorption de gluten est responsable de la DH comme de la maladie cœliaque. Le seul traitement efficace de la DH consiste, à l’instar de celui de la maladie cœliaque, en une alimentation strictement sans gluten. Pour la plupart des patients, une alimentation sans gluten entraînera la régression et la disparition des symptômes de la DH. En attendant l’effet du régime un traitement médicamenteux permet de voir diqparaître l’éruption cutanée en une semaine. Avant de pouvoir réduire la prise de médicaments, il s’écoule environ six à huit mois. Mais ce n’est qu’en excluant totalement le gluten de l’alimentation qu’on obtiendra une rémission complète ; ainsi on pourra envisager une suppression complète des médicaments dans les deux années suivantes.
Lien avec la maladie cœliaque
La DH est la manifestation cutanée spécifique de la maladie cœliaque. Un patient présentant une DH souffre de fait de la maladie cœliaque. L’inverse n’est pas nécessairement obligatoire. Chez un bon nombre de patients atteints de DH, la maladie cœliaque est si peu prononcée qu’elle passe le plus souvent inaperçue jusqu’au jour où l’éruption caractéristique apparaît. Le diagnostic de la DH se fait au moyen d’un test cutané et des méthodes classiques employées pour la maladie cœliaque (test anticorps + plus biopsie de l’intestin grêle).
Causes génétiques
La dermatite herpétiforme est dite de Dühring car c’est lui qui l’a décrite pour la première fois en 1884 comme constituant une entité clinique. En revanche son lien avec la maladie cœliaque n’a été découvert qu’à la fin des années 60. Dans les études effectuées sur les familles, on a constaté que les parents des personnes atteintes de DH développent souvent aussi une DH ou souffrent de la maladie cœliaque. Des études ont montré l’implication de gènes identiques dans les deux maladies.
Notre corps dispose de ce que l'on appelle les antigènes HLA qui déclenchent une réaction immunitaire. En cas de DH ou de maladie cœliaque, on a constaté la présence des génotypes HLA : DR3-DQ2 et DR3-DQ8. Ces antigènes prédisposent les personnes à développer une DH ou une maladie cœliaque.
Traitement de la DH
L’absorption de gluten est responsable de la DH comme de la maladie cœliaque. Le seul traitement efficace de la DH consiste, à l’instar de celui de la maladie cœliaque, en une alimentation strictement sans gluten. Pour la plupart des patients, une alimentation sans gluten entraînera la régression et la disparition des symptômes de la DH. En attendant l’effet du régime un traitement médicamenteux permet de voir diqparaître l’éruption cutanée en une semaine. Avant de pouvoir réduire la prise de médicaments, il s’écoule environ six à huit mois. Mais ce n’est qu’en excluant totalement le gluten de l’alimentation qu’on obtiendra une rémission complète ; ainsi on pourra envisager une suppression complète des médicaments dans les deux années suivantes.
Ostéoporose
Des études ont démontré que les personnes souffrant de la maladie cœliaque sont plus exposées aux fractures. Dans la plupart des cas, une faible densité minérale osseuse (DMO) en est la cause. Il s'agit donc de prendre en considération ce risque accru de fracture observé fréquemment sur des personnes souffrant de maladie cœliaque non-traitée surtout si elles ne respectent pas strictement une alimentation sans gluten. D'autres facteurs entrent en ligne de compte pour la DMO et augmentent les risques de fracture. Il est conseillé d’effectuer une ostéo-densitométrie osseuse que pour les patients s’alimentant déjà exclusivement sans gluten ainsi que pour ceux chez qui ont été décelé d‘autres facteurs de risque en dehors de la maladie cœliaque.
Troubles de la fertilité
La maladie cœliaque non-décelée ou non-traitée peut provoquer chez les femmes des troubles de la fertilité ainsi que des complications durant la grossesse, des fausses couches ou des naissances prématurées. Elle peut également entraîner une insuffisance pondérale du nouveau-né. Jusqu’à présent, on ne sait pas très bien si cette insuffisance est due à la malabsorption des éléments nutritifs en raison de l‘atrophie des villosités ou si elle masque des facteurs immunologiques.
Affections associées à la maladie cœliaque
- Déficit sélectif en IgA
- Syndrome de Sjörgen
- Cirrhose biliaire primitive
- Maladie de Crohn
- Syndrome de Down
- Syndrome de Ullrich Turner
- Syndrome de William
- Épilepsie
Formation de tumeur maligne
Le risque de voir se développer une tumeur maligne est généralement plus élevé pour les personnes souffrant de la maladie cœliaque. Les tumeurs malignes bien spécifiques de l’œsophage ou de l’intestin grêle sont les plus fréquentes. Afin de réduire ce risque, il convient d’observer une alimentation sans gluten .
Plus d'informations à ce sujet
Présentation
1
Montrer tout
Études
7
Montrer tout

Gluten and Gut-Brain Axis: Lesson Learned From Autism And Schizophrenia (2015)
Alessio Fasano, M.D.
Mucosal Immunology and Biology Research Center
Center for Celiac Research
Massachusetts General Hospital for Children
16th International Coeliac Disease Symposium 2015 à Prague
Pre-Conference Workshop on Gluten Sensitivity "The Evolving Planet of Gluten Related Disorders"
Mucosal Immunology and Biology Research Center
Center for Celiac Research
Massachusetts General Hospital for Children
16th International Coeliac Disease Symposium 2015 à Prague
Pre-Conference Workshop on Gluten Sensitivity "The Evolving Planet of Gluten Related Disorders"

Gluten and Gut-Brain Axis: Lesson Learned From Autism And Schizophrenia (2015)
Alessio Fasano, M.D.
Mucosal Immunology and Biology Research Center
...
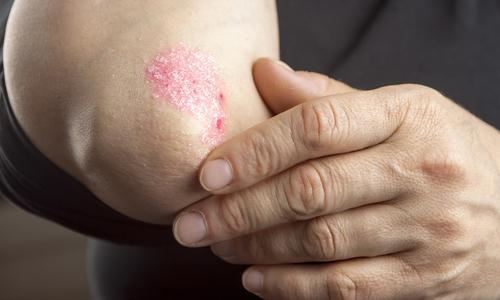
Association between Coeliac Disease and Psoriasis: Italian Primary Care Multicentre Study
Summary
Coeliac disease is increasingly associated with extraintestinal manifestations, among these, several skin disorders have been reported, with dermatitis herpetiformis being the best recognised. Several studies investigating the possible association between CD and psoriasis have been published, however results have so far proven to be inconclusive and most of the data on the effect of a gluten free diet on psoriatic skin lesions are contained within case reports.
In this prospective multicentre study, the patient records from 19 Italian primary care practices were screened for confirmed cases of psoriasis, following this 219 patients with a confirmed diagnosis of psoriasis were enrolled in to the study (111 males, 51%; mean age 54 years), and 264 age and sex matched controls without psoriasis. The severity of psoriasis amongst subjects was assessed at base-line and follow up, in addition to gastrointestinal symptoms. Serum levels of anti-tTG were recorded for all subjects and if positive, CD diagnosis was confirmed by histology on biopsy. A total of 49% of the 218 enrolled patients with psoriasis reported one or more GI symptom, the most common being heartburn/ acid regurgitation (27%) and bloating (16%). Nine out of 218 patients with psoriasis showed positive serology for CD compared to only 1 out of the 264 controls (P=<0.05). Histology confirmed the CD diagnosis in all subjects with positivity to anti-tTG antibodies. All patients with psoriasis and CD adhered to a gluten free diet and completed the 6 month follow up. At 3 months, all 9 patients showed significant improvement in the severity of their psoriasis, this improvement was maintained at 6 months in all but 1 patient whose symptoms worsened.
This study shows a significant epidemiological association between CD and psoriasis in the Italian population. However, the small number of psoriatic patients with evidence of CD cannot be considered as definitive evidence of a causal link between the two disorders. The authors of this study hypothesise that the presence of shared genes (at-risk HLA haplotypes) often used to explain the greater prevalence of CD in several autoimmune disorders, might be present in subjects affected by psoriasis. In addition, CD-related malabsorption may affect psoriasis by causing a vitamin D deficiency status. It is well known that low levels of vitamin D pre-dispose to psoriasis, and that expose to sunlight and topical vitamin D preparations improve psoriatic lesions. Furthermore, an abnormal intestinal permeability common in untreated CD may increase the passage of different immune triggers. The fact that the majority of psoriatic subjects with positive CD serology showed complete villous atrophy is concordant with the hypotheses of vitamin D malabsorption and altered intestinal permeability to the passage of immune triggers.
Resource: Dermatology 2015 Feb 3.
Coeliac disease is increasingly associated with extraintestinal manifestations, among these, several skin disorders have been reported, with dermatitis herpetiformis being the best recognised. Several studies investigating the possible association between CD and psoriasis have been published, however results have so far proven to be inconclusive and most of the data on the effect of a gluten free diet on psoriatic skin lesions are contained within case reports.
In this prospective multicentre study, the patient records from 19 Italian primary care practices were screened for confirmed cases of psoriasis, following this 219 patients with a confirmed diagnosis of psoriasis were enrolled in to the study (111 males, 51%; mean age 54 years), and 264 age and sex matched controls without psoriasis. The severity of psoriasis amongst subjects was assessed at base-line and follow up, in addition to gastrointestinal symptoms. Serum levels of anti-tTG were recorded for all subjects and if positive, CD diagnosis was confirmed by histology on biopsy. A total of 49% of the 218 enrolled patients with psoriasis reported one or more GI symptom, the most common being heartburn/ acid regurgitation (27%) and bloating (16%). Nine out of 218 patients with psoriasis showed positive serology for CD compared to only 1 out of the 264 controls (P=<0.05). Histology confirmed the CD diagnosis in all subjects with positivity to anti-tTG antibodies. All patients with psoriasis and CD adhered to a gluten free diet and completed the 6 month follow up. At 3 months, all 9 patients showed significant improvement in the severity of their psoriasis, this improvement was maintained at 6 months in all but 1 patient whose symptoms worsened.
This study shows a significant epidemiological association between CD and psoriasis in the Italian population. However, the small number of psoriatic patients with evidence of CD cannot be considered as definitive evidence of a causal link between the two disorders. The authors of this study hypothesise that the presence of shared genes (at-risk HLA haplotypes) often used to explain the greater prevalence of CD in several autoimmune disorders, might be present in subjects affected by psoriasis. In addition, CD-related malabsorption may affect psoriasis by causing a vitamin D deficiency status. It is well known that low levels of vitamin D pre-dispose to psoriasis, and that expose to sunlight and topical vitamin D preparations improve psoriatic lesions. Furthermore, an abnormal intestinal permeability common in untreated CD may increase the passage of different immune triggers. The fact that the majority of psoriatic subjects with positive CD serology showed complete villous atrophy is concordant with the hypotheses of vitamin D malabsorption and altered intestinal permeability to the passage of immune triggers.
Resource: Dermatology 2015 Feb 3.

Coeliac Disease in Women With Infertility - A Meta-Analysis
The first indications of a link between female infertility and coeliac disease was first described over 40 years ago. However, contemporary studies have failed to reach a consensus on whether patients with infertility should be screened for coeliac disease. Many studies on this subject are small, are of poor design and/ or lack a control arm. This latest meta-analysis on the subject sought to assess whether women with infertility are at higher risk of coeliac disease. Studies excluded from the meta-analysis included those without control data, those where diagnosis of coeliac disease was based only on serology, and studies where exact data regarding the number of patients included was unavailable. 105 studies were identified as a result of the initial literature search, of these only 16 were suitable for study in detail, 11 of which did not meet the inclusion criteria, leaving just 5 for inclusion in the meta-analysis to calculate the odds of having coeliac disease in women with all cause infertility and unexplained infertility. Four further studies that had been excluded on the basis that they lacked a control arm were included for calculation of the pooled prevalence of coeliac disease in women with infertility. Studies that reported coeliac disease diagnosis based on serology but with incomplete biopsy data were all included for the calculation of pooled serological prevalence of CD in women with infertility (12 studies). The meta-analysis showed that women with infertility had a 3.5 times increased odds of having coeliac disease in comparison with that in the control population. Of 422 women with unexplained infertility across the five included studies, 14 were found to have coeliac disease, representing a 6 fold increase in the odds of having coeliac disease in comparison to the control group. When data from studies without a control arm were analysed, pooled prevalence of coeliac disease amongst 884 women with all cause infertility and 623 women with unexplained infertility was 2.3% and 3.2%, respectively. Pooled serological prevalence of coeliac disease amongst women with all-cause infertility and unexplained infertility was 1.3% and 3.1%, respectively. Micronutrient deficiencies have been suggested as a possible mechanism for infertility amongst women with coeliac disease. In this meta-analysis, 28.5% of infertility patients with coeliac disease had iron deficiency in the 4 studies that reported iron status. Among the 4 studies that reported folic acid status, none of the patients with infertility and coeliac disease were deficient in this nutrient.
Although this study makes a case for screening women with infertility for coeliac disease. The authors acknowledge that their work alone cannot be used to prove a causal relationship between coeliac disease and infertility due to the limitation of the study design of case control studies, the small number of studies available overall and the small sample sizes used within these. A recent large population-based study of infertility and coeliac disease in UK women suggested that women with coeliac disease (both before and after diagnosis) do not have a greater chance of clinically recorded fertility problems than women without coeliac disease*. However, the design of this study has it's own limitations due to reliance on primary care records, the known mis-diagnosis of coeliac disease and delay in recording this within medical records.
Resource: Dhalwani N.N, West J et al (2014) Women with celiac disease present with fertility problems no more often than women in the general population. Gastroenterology 147: 1267-74
Although this study makes a case for screening women with infertility for coeliac disease. The authors acknowledge that their work alone cannot be used to prove a causal relationship between coeliac disease and infertility due to the limitation of the study design of case control studies, the small number of studies available overall and the small sample sizes used within these. A recent large population-based study of infertility and coeliac disease in UK women suggested that women with coeliac disease (both before and after diagnosis) do not have a greater chance of clinically recorded fertility problems than women without coeliac disease*. However, the design of this study has it's own limitations due to reliance on primary care records, the known mis-diagnosis of coeliac disease and delay in recording this within medical records.
Resource: Dhalwani N.N, West J et al (2014) Women with celiac disease present with fertility problems no more often than women in the general population. Gastroenterology 147: 1267-74

Causes of death in people with coeliac disease in England compared with the general population: a competing risk analysis
Abstract
Introduction:
Quantifying excess cause-specific mortality among people with coeliac disease (CD) compared with the general population accounting for competing risks will allow accurate information to be given on risk of death from specific causes.
Method:
We identified from the Clinical Practice Research Datalink all patients with CD linked to Office for National Statistics between 1998 and 2012. We selected controls by frequency matching from the registered general practice population within 10-year age bands. We calculated the adjusted cumulative incidence (including adjustment for competing risks) and excess cumulative incidence for different causes of death up to 10 years from diagnosis.
Results:
Of the 10 825 patients with CD, 773 died within the study period. The overall mortality rate among patients with CD was 128/10 000 person years compared with 153/10 000 in controls (HR=0.94 95% CI 0.84 to 1.01). We found no overall difference in the cumulative incidence of respiratory disease, digestive disease or cancer related death among cases and controls. The adjusted cumulative incidence of death from cardiovascular deaths was slightly lower compared with those without CD diagnosis (CD 0.32% vs controls 0.41%) with a corresponding excess cumulative incidence of −0.08% (95% CI −0.13 to −0.04). However, patients with CD had 0.15% excess risk (95% CI 0.03 to 0.27) of deaths from non-Hodgkin's lymphoma from the general population baseline risk.
Conclusions:
Overall, people with CD have no major excess risk of cancer, digestive disease or respiratory disease related or cardiovascular mortality compared with the general population. These findings should be reassuring to patients with CD and clinicians managing their care.
Resource: Abdul Sultan A, et al. Gut 2014;0:1–7
Alyshah Abdul Sultan, Colin J Crooks, Tim Card, Laila J Tata, Kate M Fleming, Joe West
Introduction:
Quantifying excess cause-specific mortality among people with coeliac disease (CD) compared with the general population accounting for competing risks will allow accurate information to be given on risk of death from specific causes.
Method:
We identified from the Clinical Practice Research Datalink all patients with CD linked to Office for National Statistics between 1998 and 2012. We selected controls by frequency matching from the registered general practice population within 10-year age bands. We calculated the adjusted cumulative incidence (including adjustment for competing risks) and excess cumulative incidence for different causes of death up to 10 years from diagnosis.
Results:
Of the 10 825 patients with CD, 773 died within the study period. The overall mortality rate among patients with CD was 128/10 000 person years compared with 153/10 000 in controls (HR=0.94 95% CI 0.84 to 1.01). We found no overall difference in the cumulative incidence of respiratory disease, digestive disease or cancer related death among cases and controls. The adjusted cumulative incidence of death from cardiovascular deaths was slightly lower compared with those without CD diagnosis (CD 0.32% vs controls 0.41%) with a corresponding excess cumulative incidence of −0.08% (95% CI −0.13 to −0.04). However, patients with CD had 0.15% excess risk (95% CI 0.03 to 0.27) of deaths from non-Hodgkin's lymphoma from the general population baseline risk.
Conclusions:
Overall, people with CD have no major excess risk of cancer, digestive disease or respiratory disease related or cardiovascular mortality compared with the general population. These findings should be reassuring to patients with CD and clinicians managing their care.
Resource: Abdul Sultan A, et al. Gut 2014;0:1–7
Alyshah Abdul Sultan, Colin J Crooks, Tim Card, Laila J Tata, Kate M Fleming, Joe West

Systematic review with meta-analysis: associations between coeliac disease and type 1 diabetes
Abstract
BACKGROUND:
In the past decade, a number of population-based studies have examined the prevalence of coeliac disease in individuals with type 1 diabetes but prevalences have differed considerably.
AIM:
To examine the prevalence of coeliac disease in individuals with type 1 diabetes.
METHODS:
A systematic review of English-language articles published in PubMed Medline between 2000 and May 2014. Search terms included 'celiac disease' or 'coeliac disease' and 'diabetes mellitus'. Studies were selected with at least 100 individuals with type 1 diabetes being screened for coeliac disease where the coeliac diagnosis was later confirmed through small intestinal biopsy. Data synthesis used random-effects inverse variance-weighted models, and metaregression was used to examine heterogeneity in subgroups.
RESULTS:
A pooled analysis, based on 26,605 patients with type 1 diabetes, found a prevalence of biopsy-confirmed coeliac disease of 6.0% (95% CI = 5.0-6.9%). Heterogeneity was large (I(2) = 93.2%). The prevalence was lower in adults with type 1 diabetes (2.7%), and in mixed populations with both children and adults with type 1 diabetes (4.7%) than in children (6.2%) with type 1 diabetes (P < 0.001). Additional subgroup analyses could not explain the large variation in coeliac disease prevalence between studies.
CONCLUSION:
More than one in twenty patients with type 1 diabetes have biopsy-verified coeliac disease. This prevalence is high enough to motivate screening for coeliac disease among patients with type 1 diabetes.
Resource: Aliment Pharmacol Ther. 2014 Nov;40(10):1123-32. doi: 10.1111/apt.12973. Epub 2014 Oct 1.
BACKGROUND:
In the past decade, a number of population-based studies have examined the prevalence of coeliac disease in individuals with type 1 diabetes but prevalences have differed considerably.
AIM:
To examine the prevalence of coeliac disease in individuals with type 1 diabetes.
METHODS:
A systematic review of English-language articles published in PubMed Medline between 2000 and May 2014. Search terms included 'celiac disease' or 'coeliac disease' and 'diabetes mellitus'. Studies were selected with at least 100 individuals with type 1 diabetes being screened for coeliac disease where the coeliac diagnosis was later confirmed through small intestinal biopsy. Data synthesis used random-effects inverse variance-weighted models, and metaregression was used to examine heterogeneity in subgroups.
RESULTS:
A pooled analysis, based on 26,605 patients with type 1 diabetes, found a prevalence of biopsy-confirmed coeliac disease of 6.0% (95% CI = 5.0-6.9%). Heterogeneity was large (I(2) = 93.2%). The prevalence was lower in adults with type 1 diabetes (2.7%), and in mixed populations with both children and adults with type 1 diabetes (4.7%) than in children (6.2%) with type 1 diabetes (P < 0.001). Additional subgroup analyses could not explain the large variation in coeliac disease prevalence between studies.
CONCLUSION:
More than one in twenty patients with type 1 diabetes have biopsy-verified coeliac disease. This prevalence is high enough to motivate screening for coeliac disease among patients with type 1 diabetes.
Resource: Aliment Pharmacol Ther. 2014 Nov;40(10):1123-32. doi: 10.1111/apt.12973. Epub 2014 Oct 1.

Cognitive impairment in coeliac disease improves on a gluten-free diet and correlates with histological and serological indices of disease severity
SUMMARY
Background
Mild impairments of cognition or ‘Brain fog’ are often reported by patients with coeliac disease but the nature of these impairments has not been systematically investigated.
Aim
This longitudinal pilot study investigated relationships between cognitive function and mucosal healing in people with newly diagnosed coeliac disease commencing a gluten-free diet.
Methods
Eleven patients (8 females, 3 males), mean age 30 (range 22–39) years, were tested with a battery of cognitive tests at weeks 0, 12 and 52. Information processing efficacy, memory, visuospatial ability, motoric function and attention were tested. Small bowel biopsies were collected via routine gastroscopy at weeks 12 and 52 and were compared to baseline Marsh scores. Cognitive performance was compared to serum concentrations of tissue transglutaminase antibodies, biopsy outcomes and other biological markers.
Results
All patients had excellent adherence to the diet. Marsh scores improved significantly (P = 0.001, Friedman's test) and tissue transglutaminase antibody concentrations decreased from a mean of 58.4 at baseline to 16.8 U/mL at week 52 (P = 0.025). Four of the cognitive tests assessing verbal fluency, attention and motoric function showed significant improvement over the 12 months and strongly correlated with the Marsh scores and tissue transglutaminase antibody levels (r = 0.377–0.735; all P < 0.05). However, no meaningful patterns of correlations were found for nutritional or biochemical markers, or markers of intestinal permeability.
Conclusions
In newly diagnosed coeliac disease, cognitive performance improves with adherence to the gluten-free diet in parallel to mucosal healing. Suboptimal levels of cognition in untreated coeliac disease may affect the performance of everyday tasks.
Resource: Alimentary Pharmacology & Therapeutics Volume 40, Issue 2, pages 160–170, July 2014
Background
Mild impairments of cognition or ‘Brain fog’ are often reported by patients with coeliac disease but the nature of these impairments has not been systematically investigated.
Aim
This longitudinal pilot study investigated relationships between cognitive function and mucosal healing in people with newly diagnosed coeliac disease commencing a gluten-free diet.
Methods
Eleven patients (8 females, 3 males), mean age 30 (range 22–39) years, were tested with a battery of cognitive tests at weeks 0, 12 and 52. Information processing efficacy, memory, visuospatial ability, motoric function and attention were tested. Small bowel biopsies were collected via routine gastroscopy at weeks 12 and 52 and were compared to baseline Marsh scores. Cognitive performance was compared to serum concentrations of tissue transglutaminase antibodies, biopsy outcomes and other biological markers.
Results
All patients had excellent adherence to the diet. Marsh scores improved significantly (P = 0.001, Friedman's test) and tissue transglutaminase antibody concentrations decreased from a mean of 58.4 at baseline to 16.8 U/mL at week 52 (P = 0.025). Four of the cognitive tests assessing verbal fluency, attention and motoric function showed significant improvement over the 12 months and strongly correlated with the Marsh scores and tissue transglutaminase antibody levels (r = 0.377–0.735; all P < 0.05). However, no meaningful patterns of correlations were found for nutritional or biochemical markers, or markers of intestinal permeability.
Conclusions
In newly diagnosed coeliac disease, cognitive performance improves with adherence to the gluten-free diet in parallel to mucosal healing. Suboptimal levels of cognition in untreated coeliac disease may affect the performance of everyday tasks.
Resource: Alimentary Pharmacology & Therapeutics Volume 40, Issue 2, pages 160–170, July 2014

Managing coeliac disease in patients with diabetes
Abstract
The association between coeliac disease and type 1 diabetes has long been established. The combination of genetic susceptibility along with a potential role for gluten in the pathogenesis of autoimmunity makes defining gluten's role in type 1 diabetes extremely important. Evidence supporting the role of a gluten-free diet to improve complications associated with type 1 diabetes is not robust. However there is evidence to support improved growth, bone density and potentially the prevention of additional autoimmune diseases in patients with coeliac disease and type 1 diabetes. The gluten free diet is expensive and challenging to adhere to in people already on a modified diet. Early identification of those who have coeliac disease and would benefit from a gluten-free diet is of utmost importance to prevent complications associated with type 1 diabetes and coeliac disease.
Resource: Diabetes Obes Metab. 2014 May 9
The association between coeliac disease and type 1 diabetes has long been established. The combination of genetic susceptibility along with a potential role for gluten in the pathogenesis of autoimmunity makes defining gluten's role in type 1 diabetes extremely important. Evidence supporting the role of a gluten-free diet to improve complications associated with type 1 diabetes is not robust. However there is evidence to support improved growth, bone density and potentially the prevention of additional autoimmune diseases in patients with coeliac disease and type 1 diabetes. The gluten free diet is expensive and challenging to adhere to in people already on a modified diet. Early identification of those who have coeliac disease and would benefit from a gluten-free diet is of utmost importance to prevent complications associated with type 1 diabetes and coeliac disease.
Resource: Diabetes Obes Metab. 2014 May 9

Persistent mucosal damage and risk of fracture in celiac disease.
ABSTRACT
CONTEXT:
Celiac disease (CD) is associated with an increased fracture risk, an increase that persists after diagnosis. A significant proportion of patients with CD have persistent villous atrophy (VA) on follow-up biopsy.
OBJECTIVE:
The objective of the study was to determine whether persistent VA impacts long-term fracture risk.
DESIGN:
This was a cohort study.
SETTING AND PATIENTS:
We identified all patients in Sweden with histological evidence of CD who underwent a follow-up biopsy and compared patients with persistent VA with those with mucosal healing.
MAIN OUTCOME MEASURES:
The following were measured: 1) any fracture; 2) likely osteoporotic fracture (defined as fractures of the hip, distal forearm, thoracic and lumbar spine, or proximal humerus); and 3) hip fracture.
RESULTS:
Of 7146 patients, VA was present on follow-up biopsy in 43%. There was no significant association between persistent VA and overall fractures [hazard ratio (HR) of persistent VA compared with those with healing 0.93, 95% confidence interval (CI) 0.82-1.06] or with likely osteoporotic fractures (HR 1.11, 95% CI 0.84-1.46). Persistent VA was associated with an increased risk of hip fracture (HR 1.67, 95% CI 1.05-2.66). Hip fracture risk increased, depending on the degree of VA (HR for partial VA compared with those with healing 1.70, 95% CI 0.82-3.49, HR for subtotal/total VA compared with those with healing 2.16, 95% CI 1.06-4.41).
CONCLUSIONS:
Persistent VA on follow-up biopsy is predictive of hip fracture risk. The association between persistent VA and hip fractures, but not fractures overall, implies that thinner sc tissue and fall or trauma may be mechanisms by which persistent VA confers an increased fracture risk.
Resource: J Clin Endocrinol Metab. 2014 Feb
CONTEXT:
Celiac disease (CD) is associated with an increased fracture risk, an increase that persists after diagnosis. A significant proportion of patients with CD have persistent villous atrophy (VA) on follow-up biopsy.
OBJECTIVE:
The objective of the study was to determine whether persistent VA impacts long-term fracture risk.
DESIGN:
This was a cohort study.
SETTING AND PATIENTS:
We identified all patients in Sweden with histological evidence of CD who underwent a follow-up biopsy and compared patients with persistent VA with those with mucosal healing.
MAIN OUTCOME MEASURES:
The following were measured: 1) any fracture; 2) likely osteoporotic fracture (defined as fractures of the hip, distal forearm, thoracic and lumbar spine, or proximal humerus); and 3) hip fracture.
RESULTS:
Of 7146 patients, VA was present on follow-up biopsy in 43%. There was no significant association between persistent VA and overall fractures [hazard ratio (HR) of persistent VA compared with those with healing 0.93, 95% confidence interval (CI) 0.82-1.06] or with likely osteoporotic fractures (HR 1.11, 95% CI 0.84-1.46). Persistent VA was associated with an increased risk of hip fracture (HR 1.67, 95% CI 1.05-2.66). Hip fracture risk increased, depending on the degree of VA (HR for partial VA compared with those with healing 1.70, 95% CI 0.82-3.49, HR for subtotal/total VA compared with those with healing 2.16, 95% CI 1.06-4.41).
CONCLUSIONS:
Persistent VA on follow-up biopsy is predictive of hip fracture risk. The association between persistent VA and hip fractures, but not fractures overall, implies that thinner sc tissue and fall or trauma may be mechanisms by which persistent VA confers an increased fracture risk.
Resource: J Clin Endocrinol Metab. 2014 Feb

Association between Coeliac Disease and Psoriasis: Italian Primary Care Multicentre Study
Summary
Coeliac disease is increasingly associated with extraintest...

Coeliac Disease in Women With Infertility - A Meta-Analysis
The first indications of a link between female infertility and coeliac...

Causes of death in people with coeliac disease in England compared with the general population: a competing risk analysis
Abstract
Introduction:
Quantifying excess cause-specific mortality...

Systematic review with meta-analysis: associations between coeliac disease and type 1 diabetes
Abstract
BACKGROUND:
In the past decade, a number of population-ba...

Cognitive impairment in coeliac disease improves on a gluten-free diet and correlates with histological and serological indices of disease severity
SUMMARY
Background
Mild impairments of cognition or ‘Brain fog’ ar...

Managing coeliac disease in patients with diabetes
Abstract
The association between coeliac disease and type 1 diabete...

Persistent mucosal damage and risk of fracture in celiac disease.
ABSTRACT
CONTEXT:
Celiac disease (CD) is associated with an increa...
www.drschaer-institute.com
