Sensibilité au gluten non coeliaque: un diagnostic par étapes
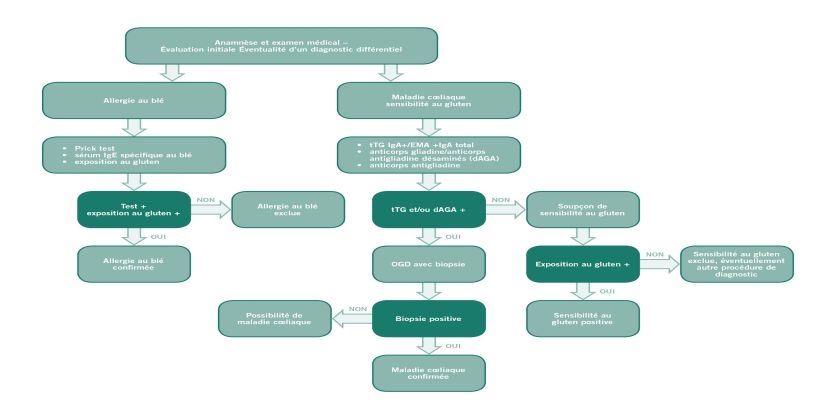
Afin d‘établir le diagnostic d’une sensibilité au gluten non coeliaque, il faut dans un premier temps exclure une maladie cœliaque ou une allergie au blé. Dans un deuxième temps, on verra si une alimentation sans gluten apporte une amélioration.
Lorsque, après avoir consommé des aliments contenant du gluten, un patient se plaint de troubles vagues : Troubles, de maux de ventre, de maux tête ou de fatigue, la première chose à faire est d’exclure une maladie cœliaque ou une allergie au blé. Le diagnostic de la sensibilité au gluten non coeliaque sera confirmé par la régression ou la disparition des symptômes dans le cadre d’un régime sans gluten et une nouvelle détérioration aussitôt après une réintroduction du gluten. Les symptômes s’estompent généralement en l’espace de quelques jours ou semaines. Il est essentiel que le patient ait une alimentation contenant du gluten avant d’effectuer le diagnostic.
Anamnèse
Évaluer les symptômes et les signes
Dans un premier temps, il est essentiel de savoir si les symptômes décrits par le patient correspondent bien à ceux de la sensibilité au gluten non coeliaque et s’ils apparaissent bien lors de la consommation d’aliments contenant du gluten. Avant d’effectuer un diagnostic, le patient doit impérativement s’alimenter normalement, c’est-à-dire consommer des produits avec du gluten.
Dans un premier temps, il est essentiel de savoir si les symptômes décrits par le patient correspondent bien à ceux de la sensibilité au gluten non coeliaque et s’ils apparaissent bien lors de la consommation d’aliments contenant du gluten. Avant d’effectuer un diagnostic, le patient doit impérativement s’alimenter normalement, c’est-à-dire consommer des produits avec du gluten.
Exclusion de la maladie cœliaque
Dosage des anticorps de la maladie cœliaque et biopsie
Les troubles de la sensibilité au gluten non coeliaque ressemblant à ceux de la maladie cœliaque, il est crucial dans un premier temps d’éliminer cette dernière. On effectuera tout d’abord un dosage des anticorps afin d’écarter un déficit en IgA. Une biopsie de l’intestin grêle permet d’exclure définitivement une maladie cœliaque. En cas de sensibilité au gluten non coeliaque, il n’y a pas d’atrophie villositaire, ou pourcentage des lymphocytes intra-épithéliaux LIE légèrement plus élevé (Marsh 0 à 1).
Les troubles de la sensibilité au gluten non coeliaque ressemblant à ceux de la maladie cœliaque, il est crucial dans un premier temps d’éliminer cette dernière. On effectuera tout d’abord un dosage des anticorps afin d’écarter un déficit en IgA. Une biopsie de l’intestin grêle permet d’exclure définitivement une maladie cœliaque. En cas de sensibilité au gluten non coeliaque, il n’y a pas d’atrophie villositaire, ou pourcentage des lymphocytes intra-épithéliaux LIE légèrement plus élevé (Marsh 0 à 1).
Exclusion de l’allergie au blé
Dosage des anticorps IgE et test cutané allergologique (prick test)
Le tableau clinique d’une allergie au blé peut ressembler à celui observé en cas de sensibilité au gluten non coeliaque. Après avoir écarté la maladie cœliaque, on pratiquera un dosage des anticorps IgE ainsi qu‘un prick test cutané afin de savoir si le patient est allergique au blé.
Le tableau clinique d’une allergie au blé peut ressembler à celui observé en cas de sensibilité au gluten non coeliaque. Après avoir écarté la maladie cœliaque, on pratiquera un dosage des anticorps IgE ainsi qu‘un prick test cutané afin de savoir si le patient est allergique au blé.
Signes complémentaires indiquant une sensibilité au gluten non coeliaque
Recherche des anticorps anti-gliadine de type IgG
La présence d’anticorps anti-gliadine de type IgG peut être révélatrice d’une sensibilité au gluten non coeliaque. On retrouve ces anticorps chez les personnes souffrant de la maladie cœliaque ainsi que chez une petite partie de la population saine. En cas de bilan histologique normal et de dosage positif des anticorps anti-gliadine de type IgG, la suspicion de sensibilité au gluten non coeliaque est renforcée.
La présence d’anticorps anti-gliadine de type IgG peut être révélatrice d’une sensibilité au gluten non coeliaque. On retrouve ces anticorps chez les personnes souffrant de la maladie cœliaque ainsi que chez une petite partie de la population saine. En cas de bilan histologique normal et de dosage positif des anticorps anti-gliadine de type IgG, la suspicion de sensibilité au gluten non coeliaque est renforcée.
Alimentation sans gluten
Régression des symptômes
Une fois la maladie cœliaque et l’allergie au blé écartées, le patient peut adopter une alimentation sans gluten. Si on est bien dans le cas d’une sensibilité au gluten non coeliaque, les symptômes régressent ou disparaissent en l’espace de quelques jours ou quelques semaines. L’alimentation sans gluten doit être prolongée durant au moins six semaines afin de pouvoir établir une corrélation entre l’alimentation sans gluten et les troubles. La régression des symptômes sera aussi évaluée en fonction d’un protocole de diagnostic élaboré lors du International Expert Meeting 2014 visant à une standardisation de la démarche. Celui-ci prévoit que le patient doit présenter avant la mise en place d’une alimentation sans gluten de un à trois des troubles importants caractéristiques et qu’il évalue leur gravité sur une échelle allant de un à dix. Cette évaluation doit avoir lieu avant la mise en place d’un régime sans gluten et être renouvelée ensuite une fois par semaine. Une réaction positive au régime sans gluten doit voir l’un des trois troubles principaux régresser d’au moins 30 % par rapport à la situation initiale. S’il n’y a pas d’aggravation des autres troubles, il doit y avoir au moins une régression de l‘un d’entre eux. Cette régression doit être d’au moins 50 % durant l’espace de temps imparti à l’évaluation, c’est-à-dire se révéler au moins dans trois des six évaluations hebdomadaires.
Une fois la maladie cœliaque et l’allergie au blé écartées, le patient peut adopter une alimentation sans gluten. Si on est bien dans le cas d’une sensibilité au gluten non coeliaque, les symptômes régressent ou disparaissent en l’espace de quelques jours ou quelques semaines. L’alimentation sans gluten doit être prolongée durant au moins six semaines afin de pouvoir établir une corrélation entre l’alimentation sans gluten et les troubles. La régression des symptômes sera aussi évaluée en fonction d’un protocole de diagnostic élaboré lors du International Expert Meeting 2014 visant à une standardisation de la démarche. Celui-ci prévoit que le patient doit présenter avant la mise en place d’une alimentation sans gluten de un à trois des troubles importants caractéristiques et qu’il évalue leur gravité sur une échelle allant de un à dix. Cette évaluation doit avoir lieu avant la mise en place d’un régime sans gluten et être renouvelée ensuite une fois par semaine. Une réaction positive au régime sans gluten doit voir l’un des trois troubles principaux régresser d’au moins 30 % par rapport à la situation initiale. S’il n’y a pas d’aggravation des autres troubles, il doit y avoir au moins une régression de l‘un d’entre eux. Cette régression doit être d’au moins 50 % durant l’espace de temps imparti à l’évaluation, c’est-à-dire se révéler au moins dans trois des six évaluations hebdomadaires.
Nouvelle exposition au gluten
Confirmation du diagnostic
Pour confirmer définitivement le diagnostic d'une sensibilité au gluten non coeliaque, il faut effectuer une nouvelle exposition au gluten comme dans tous les dépistages d’allergies alimentaires. Après une période d’un régime totalement dépourvue en gluten d‘au moins quatre semaines, le patient réintroduit du gluten dans son alimentation. Si les symptômes réapparaissent dans un délai de deux jours, on doit effectuer un test de provocation au gluten en double aveugle (études cliniques) ou en simple aveugle (cas pratiques) après plusieurs jours d’alimentation sans gluten afin de vérifier s’il ne s’agit pas d’un effet placebo. À cette fin on propose des barres de céréales sans gluten (comme placebo) et des barres contenant du gluten, lesquelles ne se différencient ni par l'aspect, la texture ou le goût.
À la première semaine test se succède une semaine de régime strict sans gluten, suivie par une deuxième semaine test. Ce protocole de diagnostic est aussi un outil d’évaluation hebdomadaire des troubles. En cas de modifications d’au moins 30% d’un des troubles identifiés par le patient entre l’introduction du gluten et celle du placebo, on peut dire qu’il s’agit d‘une sensibilité au gluten non coeliaque.
Pour confirmer définitivement le diagnostic d'une sensibilité au gluten non coeliaque, il faut effectuer une nouvelle exposition au gluten comme dans tous les dépistages d’allergies alimentaires. Après une période d’un régime totalement dépourvue en gluten d‘au moins quatre semaines, le patient réintroduit du gluten dans son alimentation. Si les symptômes réapparaissent dans un délai de deux jours, on doit effectuer un test de provocation au gluten en double aveugle (études cliniques) ou en simple aveugle (cas pratiques) après plusieurs jours d’alimentation sans gluten afin de vérifier s’il ne s’agit pas d’un effet placebo. À cette fin on propose des barres de céréales sans gluten (comme placebo) et des barres contenant du gluten, lesquelles ne se différencient ni par l'aspect, la texture ou le goût.
À la première semaine test se succède une semaine de régime strict sans gluten, suivie par une deuxième semaine test. Ce protocole de diagnostic est aussi un outil d’évaluation hebdomadaire des troubles. En cas de modifications d’au moins 30% d’un des troubles identifiés par le patient entre l’introduction du gluten et celle du placebo, on peut dire qu’il s’agit d‘une sensibilité au gluten non coeliaque.
La sensibilité au gluten non coeliaque: protocole de diagnostic
En octobre 2014, à l‘occasion des troisièmes rencontres de l’„International Expert Meeting on Non Celiac Gluten Sensitivity“, un groupe international de scientifiques et de médecins a élaboré sous la direction de Carlo Catassi et de Alessio Fasano le protocole de diagnostic décrit ci-dessus : Protocole de diagnostic. Celui-ci prévoit une démarche diététique unique en deux temps qui met en œuvre une version modifiée de la grille d’évaluation des symptômes gastro-intestinaux. Grâce à cette nouvelle grille, les patients concernés pourront évaluer les effets de l'introduction d'une alimentation sans gluten et ceux de la réintroduction du gluten sur leurs troubles. Une échelle de 1 à 10 permettra de classer les symptômes non seulement gastro-intestinaux mais aussi extra-intestinaux. Ce questionnaire facilitera l’harmonisation du diagnostic.
Plus d'informations à ce sujet
Téléchargement
1
Montrer tout
Présentation
6
Montrer tout
Études
3
Montrer tout
Vidéo
2
Montrer tout
Sensibilité au gluten non coeliaque - Une maladie sous diagnostoquée (Français)

How the diagnosis of non celiac gluten sensitivity should be confirmed: the Salerno experts’ criteria (2015)
Carlo Catassi
Department of Pediatrics
Università Politecnica delle Marche, Ancona
16th International Coeliac Disease Symposium 2015 à Prague
Pre-Conference Workshop on Gluten Sensitivity "The Evolving Planet of Gluten Related Disorders"
Department of Pediatrics
Università Politecnica delle Marche, Ancona
16th International Coeliac Disease Symposium 2015 à Prague
Pre-Conference Workshop on Gluten Sensitivity "The Evolving Planet of Gluten Related Disorders"

Biomarkers for Non-Celiac Gluten Sensitivity: A Tough, but Intriguing Challenge for Researchers (2015)
Umberto Volta
University of Bologna, Italy
16th International Coeliac Disease Symposium 2015 à Prague
Pre-Conference Workshop on Gluten Sensitivity "The Evolving Planet of Gluten Related Disorders"
University of Bologna, Italy
16th International Coeliac Disease Symposium 2015 à Prague
Pre-Conference Workshop on Gluten Sensitivity "The Evolving Planet of Gluten Related Disorders"

Diagnostic study of HLA-DQ2 typing for gluten sensitivity in IBS patients (2015)
Christian Barmeyer, Michael Schumann, Tim Meyer, Britta Siegmund, Severin Daum, Jörg-Dieter Schulzke, Reiner Ullrich
Medizinische Klinik für Gastroenterologie, Infektiologie und Rheumatologie
Charité - Universitätsmedizin Berlin
Campus Benjamin Franklin
16th International Coeliac Disease Symposium 2015 à Prague
Pre-Conference Workshop on Gluten Sensitivity "The Evolving Planet of Gluten Related Disorders"
Medizinische Klinik für Gastroenterologie, Infektiologie und Rheumatologie
Charité - Universitätsmedizin Berlin
Campus Benjamin Franklin
16th International Coeliac Disease Symposium 2015 à Prague
Pre-Conference Workshop on Gluten Sensitivity "The Evolving Planet of Gluten Related Disorders"

Gluten Sensitivity Biomarkers and Epidemiology, results from NHANES 2009–2010 (2013)
Peter H.R. Green
Celiac Disease Center
Columbia University
New York, USA
15. International Celiac Disease Symposium in Chicago between the 22nd and 25th September 2013
Celiac Disease Center
Columbia University
New York, USA
15. International Celiac Disease Symposium in Chicago between the 22nd and 25th September 2013

Gluten Sensitivity: Biomarkers and Epidemiology. The Ongoing Field Experience (2013)
Umberto Volta
Coordinator of Italian Celiac Association Board
Department of Medical and Surgical Sciences
University of Bologna, Italy
15e International Celiac Disease Symposium à Chicago du 22 au 25 septembre 2013
Coordinator of Italian Celiac Association Board
Department of Medical and Surgical Sciences
University of Bologna, Italy
15e International Celiac Disease Symposium à Chicago du 22 au 25 septembre 2013

Management of Gluten Sensitivity: Nutritional Management (2013)
Pam Cureton, RD, LD
Dietitian
Center for Celiac Research & Treatment
Boston MA, USA
15e International Celiac Disease Symposium à Chicago du 22 au 25 septembre 2013
Dietitian
Center for Celiac Research & Treatment
Boston MA, USA
15e International Celiac Disease Symposium à Chicago du 22 au 25 septembre 2013

How the diagnosis of non celiac gluten sensitivity should be confirmed: the Salerno experts’ criteria (2015)
Carlo Catassi
Department of Pediatrics
Università Politecnica delle ...

Biomarkers for Non-Celiac Gluten Sensitivity: A Tough, but Intriguing Challenge for Researchers (2015)
Umberto Volta
University of Bologna, Italy
16th International Coel...

Diagnostic study of HLA-DQ2 typing for gluten sensitivity in IBS patients (2015)
Christian Barmeyer, Michael Schumann, Tim Meyer, Britta Siegmund, Seve...

Gluten Sensitivity Biomarkers and Epidemiology, results from NHANES 2009–2010 (2013)
Peter H.R. Green
Celiac Disease Center
Columbia University
New York...

Gluten Sensitivity: Biomarkers and Epidemiology. The Ongoing Field Experience (2013)
Umberto Volta
Coordinator of Italian Celiac Association Board
Depart...

Management of Gluten Sensitivity: Nutritional Management (2013)
Pam Cureton, RD, LD
Dietitian
Center for Celiac Research & Treatment...

Diagnosis of Non-Celiac Gluten Sensitivity (NCGS): The Salerno Experts’ Criteria
Abstract
Non-Celiac Gluten Sensitivity (NCGS) is a syndrome characterized by intestinal and extra-intestinal symptoms related to the ingestion of gluten-containing food, in subjects that are not affected by either celiac disease or wheat allergy. Given the lack of a NCGS biomarker, there is the need for standardizing the procedure leading to the diagnosis confirmation. In this paper we report experts’ recommendations on how the diagnostic protocol should be performed for the confirmation of NCGS. A full diagnostic procedure should assess the clinical response to the gluten-free diet (GFD) and measure the effect of a gluten challenge after a period of treatment with the GFD. The clinical evaluation is performed using a self-administered instrument incorporating a modified version of the Gastrointestinal Symptom Rating Scale. The patient identifies one to three main symptoms that are quantitatively assessed using a Numerical Rating Scale with a score ranging from 1 to 10. The double-blind placebo-controlled gluten challenge (8 g/day) includes a one-week challenge followed by a one-week washout of strict GFD and by the crossover to the second one-week challenge. The vehicle should contain cooked, homogeneously distributed gluten. At least a variation of 30% of one to three main symptoms between the gluten and the placebo challenge should be detected to discriminate a positive from a negative result. The guidelines provided in this paper will help the clinician to reach a firm and positive diagnosis of NCGS and facilitate the comparisons of different studies, if adopted internationally.
Resource: Nutrients 2015, 7(6), 4966-4977; doi:10.3390/nu7064966
Carlo Catassi, Luca Elli, Bruno Bonaz, Gerd Bouma, Antonio Carroccio, Gemma Castillejo, Christophe Cellier, Fernanda Cristofori, Laura de Magistris, Jernej Dolinsek, Walburga Dieterich, Ruggiero Francavilla, Marios Hadjivassiliou, Wolfgang Holtmeier, Ute Körner, Dan A. Leffler,Knut E. A. Lundin, Giuseppe Mazzarella, Chris J. Mulder, Nicoletta Pellegrini, Kamran Rostami, David Sanders, Gry Irene Skodje, Detlef Schuppan, Reiner Ullrich, Umberto Volta, Marianne Williams, Victor F. Zevallos, Yurdagül Zopf and Alessio Fasano
Non-Celiac Gluten Sensitivity (NCGS) is a syndrome characterized by intestinal and extra-intestinal symptoms related to the ingestion of gluten-containing food, in subjects that are not affected by either celiac disease or wheat allergy. Given the lack of a NCGS biomarker, there is the need for standardizing the procedure leading to the diagnosis confirmation. In this paper we report experts’ recommendations on how the diagnostic protocol should be performed for the confirmation of NCGS. A full diagnostic procedure should assess the clinical response to the gluten-free diet (GFD) and measure the effect of a gluten challenge after a period of treatment with the GFD. The clinical evaluation is performed using a self-administered instrument incorporating a modified version of the Gastrointestinal Symptom Rating Scale. The patient identifies one to three main symptoms that are quantitatively assessed using a Numerical Rating Scale with a score ranging from 1 to 10. The double-blind placebo-controlled gluten challenge (8 g/day) includes a one-week challenge followed by a one-week washout of strict GFD and by the crossover to the second one-week challenge. The vehicle should contain cooked, homogeneously distributed gluten. At least a variation of 30% of one to three main symptoms between the gluten and the placebo challenge should be detected to discriminate a positive from a negative result. The guidelines provided in this paper will help the clinician to reach a firm and positive diagnosis of NCGS and facilitate the comparisons of different studies, if adopted internationally.
Resource: Nutrients 2015, 7(6), 4966-4977; doi:10.3390/nu7064966
Carlo Catassi, Luca Elli, Bruno Bonaz, Gerd Bouma, Antonio Carroccio, Gemma Castillejo, Christophe Cellier, Fernanda Cristofori, Laura de Magistris, Jernej Dolinsek, Walburga Dieterich, Ruggiero Francavilla, Marios Hadjivassiliou, Wolfgang Holtmeier, Ute Körner, Dan A. Leffler,Knut E. A. Lundin, Giuseppe Mazzarella, Chris J. Mulder, Nicoletta Pellegrini, Kamran Rostami, David Sanders, Gry Irene Skodje, Detlef Schuppan, Reiner Ullrich, Umberto Volta, Marianne Williams, Victor F. Zevallos, Yurdagül Zopf and Alessio Fasano

Celiac Disease or Non-Celiac Gluten Sensitivity? An Approach to Clinical Differential Diagnosis
Abstract
OBJECTIVES: Differentiating between celiac disease (CD) and non-celiac gluten sensitivity (NCGS) is important for appropriate management but is often challenging.
METHODS: We retrospectively reviewed records from 238 patients who presented for the evaluation of symptoms responsive to gluten restriction without prior diagnosis or exclusion of CD. Demographics, presenting symptoms, serologic, genetic, and histologic data, nutrient deficiencies, personal history of autoimmune diseases, and family history of CD were recorded. NCGS was defined as symptoms responsive to a gluten-free diet (GFD) in the setting of negative celiac serology and duodenal biopsies while on a gluten-containing diet or negative human leukocyte antigen (HLA) DQ2/DQ8 testing.
RESULTS: Of the 238 study subjects, 101 had CD, 125 had NCGS, 9 had non-celiac enteropathy, and 3 had indeterminate diagnosis. CD subjects presented with symptoms of malabsorption 67.3% of the time compared with 24.8% of the NCGS subjects (P<0.0001). In addition, CD subjects were significantly more likely to have a family history of CD (P=0.004), personal history of autoimmune diseases (P=0.002), or nutrient deficiencies (P<0.0001). The positive likelihood ratio for diagnosis of CD of a >2× upper limit of normal IgA trans-glutaminase antibody (tTG) or IgA/IgG deaminated gliadan peptide antibody (DGP) with clinical response to GFD was 130 (confidence interval (CI): 18.5–918.3). The positive likelihood ratio of the combination of gluten-responsive symptoms and negative IgA tTG or IgA/IgG DGP on a regular diet for NCGS was 9.6 (CI: 5.5–16.9). When individuals with negative IgA tTG or IgA/IgG DGP also lacked symptoms of malabsorption (weight loss, diarrhea, and nutrient deficiencies) and CD risk factors (personal history of autoimmune diseases and family history of CD), the positive likelihood ratio for NCGS increased to 80.9.
CONCLUSIONS: On the basis of our findings, we have developed a diagnostic algorithm to differentiate CD from NCGS. Subjects with negative celiac serologies (IgA tTG or IgA/IgG DGP) on a regular diet are unlikely to have CD. Those with negative serology who also lack clinical evidence of malabsorption and CD risk factors are highly likely to have NCGS and may not require further testing. Those with equivocal serology should undergo HLA typing to determine the need for biopsy.
Resource: The American Journal of Gastroenterology 109, 741-746 (May 2014)
Toufic A Kabbani, Rohini R Vanga, Daniel A Leffler, Javier Villafuerte-Galvez, Kumar Pallav, Joshua Hansen, Rupa Mukherjee, Melinda Dennis and Ciaran P Kelly
OBJECTIVES: Differentiating between celiac disease (CD) and non-celiac gluten sensitivity (NCGS) is important for appropriate management but is often challenging.
METHODS: We retrospectively reviewed records from 238 patients who presented for the evaluation of symptoms responsive to gluten restriction without prior diagnosis or exclusion of CD. Demographics, presenting symptoms, serologic, genetic, and histologic data, nutrient deficiencies, personal history of autoimmune diseases, and family history of CD were recorded. NCGS was defined as symptoms responsive to a gluten-free diet (GFD) in the setting of negative celiac serology and duodenal biopsies while on a gluten-containing diet or negative human leukocyte antigen (HLA) DQ2/DQ8 testing.
RESULTS: Of the 238 study subjects, 101 had CD, 125 had NCGS, 9 had non-celiac enteropathy, and 3 had indeterminate diagnosis. CD subjects presented with symptoms of malabsorption 67.3% of the time compared with 24.8% of the NCGS subjects (P<0.0001). In addition, CD subjects were significantly more likely to have a family history of CD (P=0.004), personal history of autoimmune diseases (P=0.002), or nutrient deficiencies (P<0.0001). The positive likelihood ratio for diagnosis of CD of a >2× upper limit of normal IgA trans-glutaminase antibody (tTG) or IgA/IgG deaminated gliadan peptide antibody (DGP) with clinical response to GFD was 130 (confidence interval (CI): 18.5–918.3). The positive likelihood ratio of the combination of gluten-responsive symptoms and negative IgA tTG or IgA/IgG DGP on a regular diet for NCGS was 9.6 (CI: 5.5–16.9). When individuals with negative IgA tTG or IgA/IgG DGP also lacked symptoms of malabsorption (weight loss, diarrhea, and nutrient deficiencies) and CD risk factors (personal history of autoimmune diseases and family history of CD), the positive likelihood ratio for NCGS increased to 80.9.
CONCLUSIONS: On the basis of our findings, we have developed a diagnostic algorithm to differentiate CD from NCGS. Subjects with negative celiac serologies (IgA tTG or IgA/IgG DGP) on a regular diet are unlikely to have CD. Those with negative serology who also lack clinical evidence of malabsorption and CD risk factors are highly likely to have NCGS and may not require further testing. Those with equivocal serology should undergo HLA typing to determine the need for biopsy.
Resource: The American Journal of Gastroenterology 109, 741-746 (May 2014)
Toufic A Kabbani, Rohini R Vanga, Daniel A Leffler, Javier Villafuerte-Galvez, Kumar Pallav, Joshua Hansen, Rupa Mukherjee, Melinda Dennis and Ciaran P Kelly

Characterization of Adults With a Self-Diagnosis of Nonceliac Gluten Sensitivity
Abstract
Background: Nonceliac gluten sensitivity (NCGS), occurring in patients without celiac disease yet whose gastrointestinal symptoms improve on a gluten-free diet (GFD), is largely a self-reported diagnosis and would appear to be very common. The aims of this study were to characterize patients who believe they have NCGS.
Materials and Methods: Advertising was directed toward adults who believed they had NCGS and were willing to participate in a clinical trial. Respondents were asked to complete a questionnaire about symptoms, diet, and celiac investigation.
Results: Of 248 respondents, 147 completed the survey. Mean age was 43.5 years, and 130 were women. Seventy-two percent did not meet the description of NCGS due to inadequate exclusion of celiac disease (62%), uncontrolled symptoms despite gluten restriction (24%), and not following a GFD (27%), alone or in combination. The GFD was self-initiated in 44% of respondents; in other respondents it was prescribed by alternative health professionals (21%), dietitians (19%), and general practitioners (16%). No celiac investigations had been performed in 15% of respondents. Of 75 respondents who had duodenal biopsies, 29% had no or inadequate gluten intake at the time of endoscopy. Inadequate celiac investigation was common if the GFD was initiated by self (69%), alternative health professionals (70%), general practitioners (46%), or dietitians (43%). In 40 respondents who fulfilled the criteria for NCGS, their knowledge of and adherence to the GFD were excellent, and 65% identified other food intolerances.
Conclusions: Just over 1 in 4 respondents self-reporting as NCGS fulfill criteria for its diagnosis. Initiation of a GFD without adequate exclusion of celiac disease is common. In 1 of 4 respondents, symptoms are poorly controlled despite gluten avoidance.
Resource: Nutr Clin Pract April 16, 2014
Jessica R. Biesiekierski, PhD, RN, Evan D. Newnham , MD, FRACP, Susan J. Shepherd, PhD, APD, Jane G. Muir, PhD, APD, Peter R. Gibson, MD, FRACP
Background: Nonceliac gluten sensitivity (NCGS), occurring in patients without celiac disease yet whose gastrointestinal symptoms improve on a gluten-free diet (GFD), is largely a self-reported diagnosis and would appear to be very common. The aims of this study were to characterize patients who believe they have NCGS.
Materials and Methods: Advertising was directed toward adults who believed they had NCGS and were willing to participate in a clinical trial. Respondents were asked to complete a questionnaire about symptoms, diet, and celiac investigation.
Results: Of 248 respondents, 147 completed the survey. Mean age was 43.5 years, and 130 were women. Seventy-two percent did not meet the description of NCGS due to inadequate exclusion of celiac disease (62%), uncontrolled symptoms despite gluten restriction (24%), and not following a GFD (27%), alone or in combination. The GFD was self-initiated in 44% of respondents; in other respondents it was prescribed by alternative health professionals (21%), dietitians (19%), and general practitioners (16%). No celiac investigations had been performed in 15% of respondents. Of 75 respondents who had duodenal biopsies, 29% had no or inadequate gluten intake at the time of endoscopy. Inadequate celiac investigation was common if the GFD was initiated by self (69%), alternative health professionals (70%), general practitioners (46%), or dietitians (43%). In 40 respondents who fulfilled the criteria for NCGS, their knowledge of and adherence to the GFD were excellent, and 65% identified other food intolerances.
Conclusions: Just over 1 in 4 respondents self-reporting as NCGS fulfill criteria for its diagnosis. Initiation of a GFD without adequate exclusion of celiac disease is common. In 1 of 4 respondents, symptoms are poorly controlled despite gluten avoidance.
Resource: Nutr Clin Pract April 16, 2014
Jessica R. Biesiekierski, PhD, RN, Evan D. Newnham , MD, FRACP, Susan J. Shepherd, PhD, APD, Jane G. Muir, PhD, APD, Peter R. Gibson, MD, FRACP

Diagnosis of Non-Celiac Gluten Sensitivity (NCGS): The Salerno Experts’ Criteria
Abstract
Non-Celiac Gluten Sensitivity (NCGS) is a syndrome character...

Celiac Disease or Non-Celiac Gluten Sensitivity? An Approach to Clinical Differential Diagnosis
Abstract
OBJECTIVES: Differentiating between celiac disease (CD) an...

Characterization of Adults With a Self-Diagnosis of Nonceliac Gluten Sensitivity
Abstract
Background: Nonceliac gluten sensitivity (NCGS), occurring...
NCGS: are we moving from a diagnosis of exclusion to a positive diagnosis?
Professor Carlo Catassi
Gastroenterologist Pediatrician
Department of Pediatrics
Università Politecnica delle Marche
60123 Ancona, Italy
At the Expert Meeting 2014 in Salerno, Italy.
Gastroenterologist Pediatrician
Department of Pediatrics
Università Politecnica delle Marche
60123 Ancona, Italy
At the Expert Meeting 2014 in Salerno, Italy.
Are we moving from a diagnosis of exclusion to a positive diagnosis?
Reiner Ullrich, MD
Universitätsmedizin Berlin
Campus Benjamin Franklin,
Medizinische Klinik für Gastroenterologie
12203 Berlin, Germany
At the Expert Meeting 2014 in Salerno, Italy
Universitätsmedizin Berlin
Campus Benjamin Franklin,
Medizinische Klinik für Gastroenterologie
12203 Berlin, Germany
At the Expert Meeting 2014 in Salerno, Italy

NCGS: are we moving from a diagnosis of exclusion to a positive diagnosis?
Professor Carlo Catassi
Gastroenterologist Pediatrician
Department o...

Are we moving from a diagnosis of exclusion to a positive diagnosis?
Reiner Ullrich, MD
Universitätsmedizin Berlin
Campus Benjamin Frankl...
www.drschaer-institute.com
